题目内容
6.取两个相同容积的密闭恒容容器,在A容器中充入0.2molN2O4,B容器中充入0.2molHI气体,在一定温度下反应分别达到平衡,测得N2O4和HI的分解率分别为a(A)和a(B).在该平衡体系中再分别充入0.2molN2O4和0.2molHI,当反应重新达到平衡时,测得N2O4和HI的分解率分别为a′(A)和a′(B).下列判断一定正确的是( )| A. | a(A)>a′(A) a(B)<a′(B) | B. | a(A)>a′(A) a(B)=a′(B) | C. | a(A)<a′(A) a(B)<a′(B) | D. | a(A)=a′(A) a(B)>a′(B) |
分析 A容器中N2O4?2NO2,B容器中2HI(g)?H2(g)+I2(g),恒容容器中,再充入0.2molN2O4和0.2molHI,容器内压强增大,A中正反应气体体积增大,反应物转化率降低,B中反应前后气体体积不变,转化率不变,据此分析.
解答 解:A容器中N2O4?2NO2,B容器中2HI(g)?H2(g)+I2(g),恒容容器中,再充入0.2molN2O4和0.2molHI,容器内压强增大,A中正反应气体体积增大,反应物转化率降低,所以α(A)>α′(A),B中反应前后气体体积不变,转化率不变,即a(B)=a′(B),故选B.
点评 本题以二氧化氮和四氧化二氮的可逆反应以及碘化氢的分解反应为载体考查了化学平衡移动原理,要注意:压强只对反应前后气体体积改变的可逆反应平衡移动有影响,对反应前后气体体积不变化的可逆反应无影响,但压强对所有有气体参加的可逆反应反应速率都有影响,无论反应前后气体体积是否变化.

练习册系列答案
相关题目
9.能区别硝酸银、盐酸、氢氧化钾三种溶液的一种试剂是( )
| A. | MgCl2溶液 | B. | FeCl3溶液 | C. | NaNO3溶液 | D. | K2SO4溶液 |
10.镍-镉可充电电池可发生如下反应:Cd(OH)2$?_{放电}^{充电}$+2Ni(OH)2充电放电Cd+2NiO(OH)+2H2O由此可知,该电池的负极材料是( )
| A. | Cd | B. | NiO(OH) | C. | Cd(OH)2 | D. | Ni(OH)2 |
1.一定温度下,将3mol PCl3和 1.5mol Cl2充入容积不变的密闭容器中,在一定条件下反应:PCl3+Cl2?PCl5.各物质均为气态.达平衡后,PCl5为0.4mol.若此时再移走1.5mol PCl3 和0.75mol Cl2,相同温度下达到平衡,PCl5的物质的量为( )
| A. | 0.4mol | B. | 0.2mol | C. | 0.2mol<x<0.4mol | D. | <0.2mol |
11.现有几组物质的熔点数据如下表:
据此回答下列问题:
(1)A组属于原子晶体晶体,其熔化时克服的微粒间的作用力是共价键;
(2)B组晶体共同的物理性质是①②③④(填序号);①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间存在氢键;
(4)D组晶体可能具有的性质是②④(填序号);①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
| A组 | B组 | C组 | D组 |
| 金刚石:3110℃ | Li:181℃ | HF:-83℃ | NaCl:801℃ |
| 硅晶体:1410℃ | Na:98℃ | HCl:-114℃ | KCl:776℃ |
| 硼晶体:2300℃ | K:64℃ | HBr:-89℃ | RbCl:718℃ |
| 二氧化硅:1723℃ | Rb:39℃ | HI:-51℃ | CsCl:645℃ |
(1)A组属于原子晶体晶体,其熔化时克服的微粒间的作用力是共价键;
(2)B组晶体共同的物理性质是①②③④(填序号);①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间存在氢键;
(4)D组晶体可能具有的性质是②④(填序号);①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
16.捕碳技术是指从空气中捕获CO2的技术.目前NH3已经被用作工业捕碳剂.下列物质中不能作为捕碳剂的是( )
| A. | 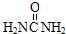 | B. | H2NCH2CH2NH2 | C. | (NH4)2CO3 | D. | Na2CO3 |
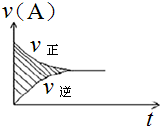 可逆反应aA(g)+bB(g)?cC(g)+dD(g)的v-t图象如图所示.
可逆反应aA(g)+bB(g)?cC(g)+dD(g)的v-t图象如图所示.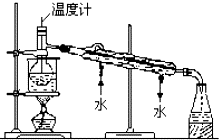 海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题:
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题: