题目内容
18.某学生课外活动小组模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积.图中量气装置E由甲乙两根玻璃管组成,它们由橡皮管连通,并装入适量水.甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低.实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水.
请回答:
(1)图中各装置接口连接顺序是:(填各接口的编号,其中连接胶管及夹持装置均省略)
⑤→③→④→⑥→⑦→②→①→⑧
(2)装置C中放入的反应物是CaCO3和HCl(填化学式).
(3)装置B的作用是吸收CO2中混有的HCl.
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数求其差值的过程中,应注意ab和c(填字母编号).
a.视线与凹液面最低处相平
b.等待气体恢复常温才读数
c.读数时应上下移动乙管,使甲乙两管液面相平
d.读数时不一定使甲乙两管液面相平
(5)实验测收集的氧气在标准状况下体积为V L,则参与反应的Na2O2 的物质的量为$\frac{V}{11.2}$mol.
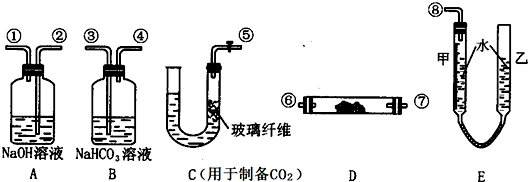
分析 题目要求利用过氧化钠与二氧化碳(潮湿)反应制取氧气,故首先需要制备二氧化碳.只有仪器C可以用来制取二氧化碳.制气原料应该采用大理石和盐酸,此法制得的二氧化碳中会含有少量氯化氢.须通过装有碳酸氢钠溶液的洗气瓶,以除去这些氯化氢.然后使净化后的二氧化碳通过过氧化钠来制取氧气,该仪器只能选用装置D.此反应属于气体与固体之间的反应,不易反应完全,为了除去生成的氧气中混有未反应的二氧化碳,可以使它们通过仪器A.在测量氧气体积时,为了使测量更为准确,要注意上下移动仪器E中的乙管,使甲、乙两管的液面相平,以使甲管中的气压与大气气压相等,同时视线应与甲管内凹液面最低处相平,以减少观察误差.最后根据方程式计算过氧化钠的物质的量.
解答 解:(1)仪器C可以用来制取二氧化碳,连接③用来除去HCl,④连接⑥可使二氧化碳与过氧化钠反应生成氧气,然后连接②可除去未反应的二氧化碳,最后连接⑧测量气体的体积,所以顺序为⑤③④⑥⑦②①⑧,
故答案为:⑤;③;④;②;①;⑧;
(2)碳酸钙与盐酸反应生成二氧化碳,所以装置C中加入碳酸钙和盐酸制备二氧化碳;
故答案为:CaCO3;HCl;
(3)仪器C可以用来制取二氧化碳,此法制得的二氧化碳中会含有少量氯化氢,须通过装有碳酸氢钠溶液的洗气瓶,以除去这些氯化氢;
故答案为:吸收CO2中混有的HCl;
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数.求其差值的过程中,
应注意:①等待气体恢复常温才读数;②读数时要调节E中甲乙的液面使其同一高度;③读数时视线要与凹液面最低处相平,
故答案为:ab;c;
(5)依据过氧化钠与二氧化碳反应的方程式计算产生参加反应的过氧化钠的物质的量:
2Na2O2+2CO2=2Na2CO3+O2↑,
2mol 22.4L
n VL
解得:n=$\frac{V}{11.2}$mol,
故答案为:$\frac{V}{11.2}$.
点评 本题考查过氧化钠与二氧化碳的反应,并考查气体的制备、除杂、量气等知识,把握实验原理和操作方法是解题关键,题目难度中等.

| A. | MgCl2溶液 | B. | FeCl3溶液 | C. | NaNO3溶液 | D. | K2SO4溶液 |
| A. | 0.2 mol/L | B. | 0.3 mol/L | C. | 0.4 mol/L | D. | 0.6 mol/L |
| A. | 分子中碳原子不在一条直线上 | B. | 光照不能够发生取代反应 | ||
| C. | 是石油分馏的一种产品 | D. | 比丁烷更易液化 |
| A. | Cd | B. | NiO(OH) | C. | Cd(OH)2 | D. | Ni(OH)2 |
 化学与社会经济建设、生态文明建设、人类健康保障、环境保护等密切相关.
化学与社会经济建设、生态文明建设、人类健康保障、环境保护等密切相关.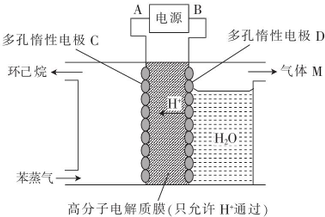 氢能的研究和利用是当今科学研究的热点之一,而寻找性能优越,安全性高、价格低廉、环保的储氢
氢能的研究和利用是当今科学研究的热点之一,而寻找性能优越,安全性高、价格低廉、环保的储氢
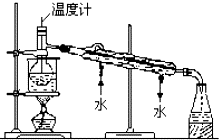 海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题:
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题: