题目内容
20.(1)下列△H表示物质燃烧热的是△H3;表示中和热△H=-57.3kJ•mol-1的是△H5.(填“△H1”、“△H2”和“△H3”等),△H1>△H3(填“>”、“<”或“=”)A.C(s)+1/2O2(g)=CO(g)△H1
B.2H2(g)+O2(g)=2H2O(l)△H2
C.C(s)+O2(g)=CO2(g)△H3
D.$\frac{1}{2}$Ba(OH)2(aq)+$\frac{1}{2}$H2SO4(aq)=$\frac{1}{2}$BaSO4(s)+H2O(l)△H4
E.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H5
F.2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H6
(2)在25℃、101kPa下,0.2mol液态甲醇燃烧生成CO2 气体和液态水时放热144.0kJ.则表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-720.0kJ•mol-1.
(3)用“>”、“<”或“=”填空:
①同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的热效应(化学计量数相同)分别为△H1、△H2,则△H1=△H2.
②相同条件下,2mol氢原子所具有的能量>1mol 氢分子所具有的能量.
③等质量的硫蒸汽、硫磺、分别在足量空气中燃烧所对应的热效应分别为△H1、△H2则△H1<△H2.
分析 (1)根据燃烧热、中和热的定义,燃烧热指1mol可燃物完全燃烧生成稳定的化合物时所放出的热量,中和热是指酸碱中和反应生成1mol水放出的热量,据此答题;
(2)计算甲醇的物质的量,计算1mol甲醇燃烧放出的热量,进而可写出表示甲醇燃烧热的热化学方程式;
(3)①反应热与反应物的总能量和生成物的总能量,与反应条件无关;
②化学键断裂为吸热过程;
③常温时硫磺比硫蒸汽稳定,说明等质量的硫蒸汽能量高,硫蒸汽反应放出的热量较多;
解答 解:(1)燃烧热指1mol可燃物完全燃烧生成稳定的化合物时所放出的热量,反应C为燃烧热的热化学方程式,中和热是指酸碱中和反应生成1mol水放出的热量,只有E符合,根据反应A和C,1mol碳燃烧生成一氧化碳所放出的热量小于生成二氧化碳所放出的热量,所以△H1>△H3,
故答案为:△H3;△H5;>;
(2)0.2mol液态甲醇燃烧生成CO2 气体和液态水时放热144.0kJ,则1mol甲醇燃烧生成CO2和液态水时放热144.0kJ×5=720kJ,表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-720.0kJ•mol-1,
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-720.0kJ•mol-1;
(3)①反应热与反应物的总能量和生成物的总能量,与反应条件无关,则光照和点燃条件的△H相同,
故答案为:=;
②氢气分子生成氢原子要破坏化学键,需要吸热,则2mol氢原子所具有的能量大于1mol氢分子所具有的能量,
故答案为:>;
③常温时硫磺比硫蒸汽稳定,说明等质量的硫蒸汽能量高,硫蒸汽反应放出的热量较多,因△H<0,则放出的能量越多反应热越小,
故答案为:<.
点评 本题综合考查反应热的大小比较以及影响化学平衡的因素,题目难度不大,注意把握比较反应热的角度.

| A. | Na2O与Na2O2均可与盐酸反应,故二者皆为碱性氧化物 | |
| B. | Na2O与Na2O2不可以相互转化 | |
| C. | 取一块金属钠放在燃烧匙里加热,金属先熔化,燃烧时火焰呈黄色,生成淡黄色固体 | |
| D. | 在呼吸面具中,Na2O2常作供氧剂,而Na2O不能 |
| A. | 物质的量就是物质的质量 | |
| B. | 物质的量不是国际单位制的七个基本物理量之一 | |
| C. | 物质的量是摩尔的单位 | |
| D. | 阿伏加德罗常数的数值约为6.02×1023 |
ⅠAⅡAⅢAⅣAⅤAⅥAⅦA0周期族
(1)将B中所含元素填写在如表的恰当位置中(用元素符号表示)
| 1 | ||||||||
| 2 | ||||||||
| 3 |
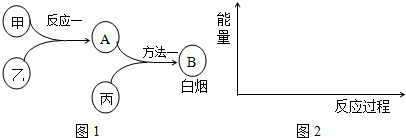
(3)为加快反应一的速率,可采取的措施有:适当升高温度、选用恰当的催化剂、增大某一反应物的浓度和增大压强.
(4)方法一的化学方程式是3Cl2+8NH3=N2+6NH4Cl.
(5)用方法二也能制得B:甲和丙反应的产物与A反应即可,这两种方法更好的是方法二(填“方
法一”或“方法二”),理由是方法二的原子利用率100%,零排放,符合绿色化学理念.
| A. | X的分解速率是Y的消耗速率 的2倍 | |
| B. | 混合气体的压强不再变化 | |
| C. | 混合气体的密度不再变化 | |
| D. | 单位时间内生成lmolY的同时分解2mol X |
| A. | 溶质电离方程式为NaHCO3═Na++H++CO32- | |
| B. | 25℃时,加水稀释后,n(H+)与n(OH-)的乘积变大 | |
| C. | 离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 温度升高,c(HCO3-)增大 |