题目内容
3.若要使0.5mol甲烷完全和氯气发生取代反应,并生成相同物质的量的四种取代物,则需要氯气的物质的量为( )| A. | 2.5 mol | B. | 2 mol | C. | 1.25 mol | D. | 0.5 mol |
分析 根据四种取代物的物质的量相等结合碳原子守恒计算取代物的物质的量,再根据被取代的氢原子和氯气分子之间的关系式计算消耗氯气的物质的量.
解答 解:4种氯代烃的物质的量相等,即各有$\frac{0.5}{4}$mol=0.125mol,由于氯气发生的取代反应是1个氯原子替换出1个氢原子,另一个氯原子则与氢原子结合生成氯化氢,所以参加反应的氯气的物质的量等于生成的氯代烃中氯原子的物质的量,所以所需的氯气的物质的量为0.125mol×1+0.125mol×2+0.125mol×3+0.125mol×4=1.25mol,
故选C.
点评 本题考查了甲烷的取代反应,明确甲烷的取代反应中被取代的氢原子和氯气之间的关系是解本题的关键,难度不大.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
13.向平衡体系2NO+O2═2NO2中,通入18O组成的氧气,重新达到平衡后,18O存在于( )
| A. | 仅在O2中 | B. | 仅在NO2中 | C. | 仅在O2和NO2中 | D. | 平衡体系中 |
11.关于Li原子结构和性质的判断如下:①与H2O反应比Na剧烈;②它的原子半径比Na小;③它的氧化物暴露在空气中易吸收H2O和CO2;④它的阳离子最外层电子数和钠离子的最外层电子数相同;⑤它在反应中只能作还原剂;⑥Li应保存在煤油中,以隔绝空气;⑦Li在空气中燃烧生成Li2O2.其中错误的组合是( )
| A. | ①④⑥⑦ | B. | ①②③ | C. | ③⑤⑥ | D. | ①⑥⑦ |
18.在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
| A. | 正极附近的S042-离子浓度逐渐增大 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 铜片上有H2逸出 | |
| D. | 溶液的pH逐渐变小 |
8.下列关于物质性质变化的比较中正确的( )
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③热稳定性:HCl>H2S>PH3
④还原性:F->Cl->Br-.
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③热稳定性:HCl>H2S>PH3
④还原性:F->Cl->Br-.
| A. | ①②④ | B. | ②③④ | C. | ①②③ | D. | ①②③④ |
12.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体.它的分子是三角锥形,以下关于PH3的叙述正确的是( )
| A. | PH3是非极性分子,难溶于水 | |
| B. | PH3的熔沸点高于NH3,极易被液化 | |
| C. | PH3稳定性弱于NH3,是因为NH3分子间还存在氢键 | |
| D. | PH3分子中有未成键的孤对电子 |
13.含有一个-C≡C-的炔烃与氢气发生加成反应后的产物的结构简式如图所示,此炔烃可能的结构有( )
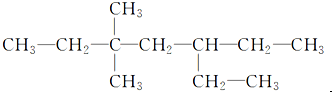
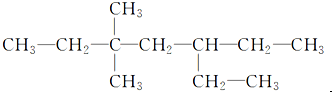
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
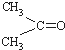 )与两个烃基相连的化合物叫酮(如丙酮 ).下列醇能发生脱氢氧化,但不可能得到醛类化合物的是( )
)与两个烃基相连的化合物叫酮(如丙酮 ).下列醇能发生脱氢氧化,但不可能得到醛类化合物的是( )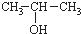
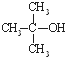
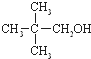
 回答下列问题:
回答下列问题: