题目内容
12.膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体.它的分子是三角锥形,以下关于PH3的叙述正确的是( )| A. | PH3是非极性分子,难溶于水 | |
| B. | PH3的熔沸点高于NH3,极易被液化 | |
| C. | PH3稳定性弱于NH3,是因为NH3分子间还存在氢键 | |
| D. | PH3分子中有未成键的孤对电子 |
分析 A、PH3分子中存在P-H极性键,分子结构不对称,为极性分子;
B、NH3中存在氢键,导致其沸点反常的升高;
C、气态氢化物的稳定性与化学键有关,与氢键无关;
D、PH3中P原子成3个σ键,有一对未成键的孤对电子.
解答 解:A、PH3分子中三个P-H键完全相同,所以键能、键长,键角都相等;分子中P-H键是不同非金属元素之间形成的极性共价键,该分子为三角锥型结构,分子结构不对称,为极性分子,根据相似相溶原理,应易溶于水,故A错误;
B、NH3中存在氢键,导致其沸点反常的比PH3的沸点更高,即NH3更易液化,故B错误;
C、N-H键的键能较P-H键的键能大,则NH3的稳定性更强,氢键只影响物质的熔沸点,与物质的稳定性无关,故C错误;
D、分子中除了用于形成共价键的键合电子外,还经常存在未用于形成共价键的非键合电子.这些未成键的价电子对叫做孤对电子,PH3的P原子最外层满足8电子结构,P上连有3个氢,有一对孤对电子,故D正确;
故选D.
点评 本题以膦为载体考查了物质的结构、化学键等知识点,以氨气分子为例采用知识迁移的方法进行分析解答,注意结合基本概念分析,题目难度中等.

练习册系列答案
相关题目
2.下列各有机物的分类或命名正确的是( )
| A. | 对甲基苯酚属于芳香烃 | B. | 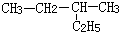 2-乙基丁烷 2-乙基丁烷 | ||
| C. | 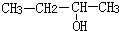 3-丁醇 3-丁醇 | D. | 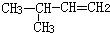 3-甲基-1-丁烯 3-甲基-1-丁烯 |
3.若要使0.5mol甲烷完全和氯气发生取代反应,并生成相同物质的量的四种取代物,则需要氯气的物质的量为( )
| A. | 2.5 mol | B. | 2 mol | C. | 1.25 mol | D. | 0.5 mol |
20.下列化合物中既有离子键又有共价键的是( )
| A. | CaBr2 | B. | Na2O2 | C. | HBr | D. | N2 |
17.下列有关酸雨的说法正确的是( )
| A. | 酸雨就是指pH<7的雨水 | |
| B. | 工业上大量燃烧含硫燃料和以含硫矿石为原料冶炼金属产生的SO2是产生硫酸型酸雨的主要原因 | |
| C. | 酸雨是因为雨水中含有CO2 | |
| D. | 酸雨没有危害,所以不必担心,也不必想办法治理 |
4.下列叙述中错误的是( )
| A. | 苯与浓硝酸、浓硫酸共热并保持50~60℃反应生成硝基苯 | |
| B. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 用乙醇和3%的硫酸共热到170℃制取乙烯 |
1.下列关于能量转化的认识中错误的是( )
| A. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| B. | 绿色植物进行光合作用时,太阳能转化为化学能 | |
| C. | 电池充电是将电能转化为化学能 | |
| D. | 燃料电池的能量转化率可达100% |
3.CoxFe3-xO4磁粉是一种比较好的高矫顽力磁粉.工业上以FeSO4为原料制备CoxFe3-xO4的主要步骤如下:
FeSO4$\stackrel{①}{→}$FeOOH晶种$\stackrel{②}{→}$FeOOH$\stackrel{③}{→}$Fe2O3$\stackrel{④}{→}$Fe3O4$→_{⑤}^{CoSO_{4}溶液}$
(1)步骤①是在FeSO4溶液中加入NaOH溶液,在40℃下搅拌生成FeOOH晶种.生成晶种的化学方程式为4FeSO4+8NaOH+O2$\frac{\underline{\;40℃\;}}{\;}$4FeOOH+4Na2SO4+2H2O;
(2)步骤③将FeOOH固体在200~300℃下加热脱水,生成红色Fe2O3.实验室完成该操作需要下列仪器中的cde(填字母).
a.蒸发皿 b.烧杯 c.坩埚 d.泥三角 e.酒精灯
(3)步骤④通入H2,加热至300~400℃,生成Fe3O4.通入H2前要向加热炉中通入N2,其作用为排尽装置中的空气,防止氢气与氧气混合反应爆炸.
(4)步骤⑤加入CoSO4溶液,所得粗产品经过滤、洗涤、干燥即得成品.检验粗产品洗涤干净的实验操作和现象是取最后一次洗涤滤出液少许于试管中,滴加氯化钡溶液,如果不产生白色沉淀,则表明洗涤干净.
(5)某研究小组欲用锂离子电池正极废料(含LiCoO2、铝箔、铁的氧化物)制备CoSO4•7H2O晶体.下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
请完成下列实验步骤(可选用的试剂:H2O2、稀硝酸、稀硫酸、NaOH溶液).
①用N-甲基吡咯烷酮在120℃下浸洗正极废料,使LiCoO2与铝箔分离,得到LiCoO2粗品并回收铝.
②用稀硫酸溶解LiCoO2,并加入过量H2O2.
③向所得粗品CoSO4溶液中加入NaOH溶液,调节pH约为5,过滤.
④向③所得滤液中加入NaOH溶液,调节pH至9.4,过滤,洗涤得到Co(OH)2沉淀.
⑤将Co(OH)2沉淀溶于稀硫酸中,蒸发浓缩、降温结晶,得到CoSO4•7H2O晶体.
FeSO4$\stackrel{①}{→}$FeOOH晶种$\stackrel{②}{→}$FeOOH$\stackrel{③}{→}$Fe2O3$\stackrel{④}{→}$Fe3O4$→_{⑤}^{CoSO_{4}溶液}$
(1)步骤①是在FeSO4溶液中加入NaOH溶液,在40℃下搅拌生成FeOOH晶种.生成晶种的化学方程式为4FeSO4+8NaOH+O2$\frac{\underline{\;40℃\;}}{\;}$4FeOOH+4Na2SO4+2H2O;
(2)步骤③将FeOOH固体在200~300℃下加热脱水,生成红色Fe2O3.实验室完成该操作需要下列仪器中的cde(填字母).
a.蒸发皿 b.烧杯 c.坩埚 d.泥三角 e.酒精灯
(3)步骤④通入H2,加热至300~400℃,生成Fe3O4.通入H2前要向加热炉中通入N2,其作用为排尽装置中的空气,防止氢气与氧气混合反应爆炸.
(4)步骤⑤加入CoSO4溶液,所得粗产品经过滤、洗涤、干燥即得成品.检验粗产品洗涤干净的实验操作和现象是取最后一次洗涤滤出液少许于试管中,滴加氯化钡溶液,如果不产生白色沉淀,则表明洗涤干净.
(5)某研究小组欲用锂离子电池正极废料(含LiCoO2、铝箔、铁的氧化物)制备CoSO4•7H2O晶体.下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Co2+ | 6.9 | 9.4 |
①用N-甲基吡咯烷酮在120℃下浸洗正极废料,使LiCoO2与铝箔分离,得到LiCoO2粗品并回收铝.
②用稀硫酸溶解LiCoO2,并加入过量H2O2.
③向所得粗品CoSO4溶液中加入NaOH溶液,调节pH约为5,过滤.
④向③所得滤液中加入NaOH溶液,调节pH至9.4,过滤,洗涤得到Co(OH)2沉淀.
⑤将Co(OH)2沉淀溶于稀硫酸中,蒸发浓缩、降温结晶,得到CoSO4•7H2O晶体.