题目内容
19.化学无处不在,下列说法正确的是( )| A. | 工业上制取玻璃的工艺是应用了物质酸性的差异 | |
| B. | 家庭里可用淀粉检验加碘盐是否含有碘 | |
| C. | 铁是人体必需的微量元素,所以可以适当地吃点铁锈 | |
| D. | 王水是由浓盐酸和浓硝酸两种物质按3:1的体积比混合配制成的 |
分析 A.二氧化硅能与碳酸钠反应生成硅酸钠和二氧化碳;
B.淀粉遇单质碘变蓝;
C.二价铁易被人体吸收;
D.王水是浓盐酸和浓硝酸按3:1的体积比组成的混合物.
解答 解:A.二氧化硅能与碳酸钠反应生成硅酸钠和二氧化碳,是难挥发性酸制取易挥发性酸,故A错误;
B.淀粉遇单质碘变蓝,而食用加碘盐为KIO3,不能用来检验,故B错误;
C.二价铁易被人体吸收,铁锈含有三价铁,故C错误;
D.王水是浓盐酸和浓硝酸按3:1的体积比组成的混合物,能溶解金、铂,故D正确.
故选D.
点评 本题考查物质的检验和制备、组成等,题目难度不大,本题注意碘盐的组成、注意补铁的方法.

练习册系列答案
相关题目
16.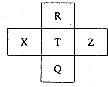 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )| A. | X元素的最高价氧化物对应的水化物酸性强于T元素 | |
| B. | 原子半径:R<T<Z | |
| C. | Z的单质可从T的气态氢化物中置换出T的单质 | |
| D. | R、T、Q最高正价相同 |
10.下列物质的变化过程中,有共价键明显被破坏的是( )
| A. | I2升华 | B. | NaCl颗粒被粉碎 | ||
| C. | H2SO4溶于水得硫酸溶液 | D. | NaOH受热熔化 |
14.下列物质的性质比较中正确的是( )
| A. | 键的极性:H2O>H2S | B. | 导电性:HF溶液<HCl溶液 | ||
| C. | 燃烧热:△H(C)(s,石墨)>△H(CO)(g) | D. | 耐腐蚀性:铝<生铁 |
11.美国《Science》杂志曾经报道:在40GPa高压下,用激光器加热到1800K,人们成功制得了原子晶体干冰.有关原子晶体干冰的推断错误的是( )
| A. | 有很高的熔点和沸点 | B. | 易汽化,可用作制冷材料 | ||
| C. | 含有极性共价键 | D. | 硬度大,可用作耐磨材料 |
8.在含有0.6molCl-、0.8molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.则( )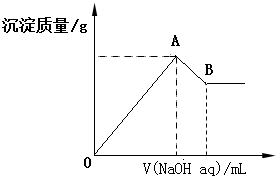

| A. | x=$\frac{2a}{5-a}$ | |
| B. | x的取值范围是0<x<$\frac{11}{32}$ | |
| C. | A点横坐标的值随x发生变化 | |
| D. | 若B点横坐标为200mL时,c(NaOH)=7.0mol/L |
9.在下列实验中,应将温度计插入水浴中的是( )
| A. | 在实验室中蒸馏石油 | B. | 由苯制硝基苯 | ||
| C. | 由酒精制乙烯 | D. | 由乙酸与乙醇反应制乙酸乙酯 |
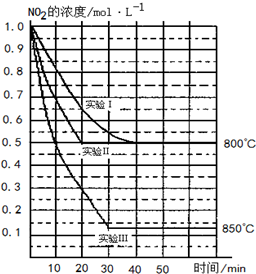 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol•L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol•L-1)随时间(min)的变化如图所示.请回答下列问题: