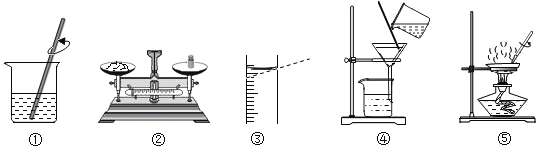
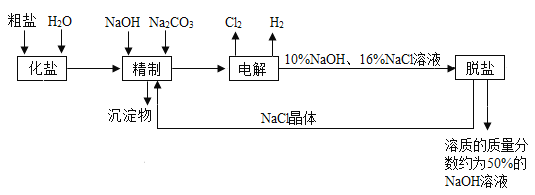
【题目】酸和碱作用生成盐和水的反应叫中和反应。某化学兴趣小组同学对“盐酸 中和氢氧化钠溶液”的反应进行探究。
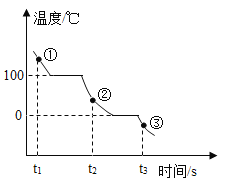
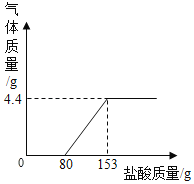
(1)小明在做“盐酸中和氢氧化钠溶液”的实验时,测出反应过程中溶液的 pH 变化如图所示。
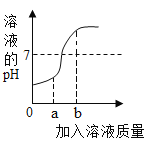
①该反应的化学方程式为:___________。
②该实验操作是将_________滴加到另一种溶液中。
③当加入溶液的质量为 ag 时,所得溶液中的阳离子有(写符号)_____________。
④当加入溶液的质量为 bg 时,向所得溶液溶液中滴入紫色石蕊试液,紫色石蕊试液变________色。
(2)小亮在做“盐酸中和氢氧化钠溶液”的实验时,向氢氧化 钠溶液里滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度,于是他 对所得溶液的酸碱性进行探究。
(探究目的)探究所得溶液的酸碱性。
(提出猜想)所得溶液可能呈酸性,也可能呈___________性,还可能呈碱性。
(实验验证)
实验操作 | 实验现象 | 结论 |
用试管取该溶液 1-2mL,滴入 1-2滴无色酚酞试液,振荡。 | 无色酚酞试液变______________色。 | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈__________。 |
(交流与反思)
①若溶液呈碱性,则溶液中使其呈碱性的离子是__________(写符号)。
②若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:取样,加入_____________,若有______________现象,则呈酸性;若无明显现象,则呈中性。
【题目】化学实验过程经常会产生定量的废液,经过无害化处理可有效防止水体污染。在一次实验课上,兴趣小组的同学们完成了NaOH溶液和Na2CO3溶液的鉴别,并对废液成分展开探究。
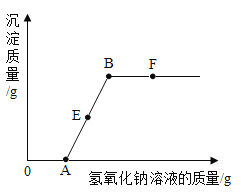
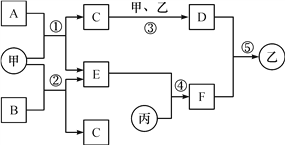
活动一 通过小组合作,同学们完成了如图所示的三组小实验。实验中生成白色沉淀的化学方程式是_(写一个)。
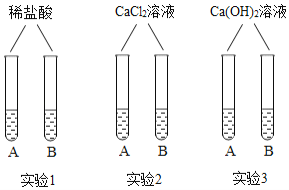
活动二 小雪将六支试管中的剩余物倒入一个洁净的大烧杯中(如图),充分搅拌、静置,观察到杯内上层是无色溶液,下层有白色沉淀。由此可以确定:上层溶液中一定不含有的离子是_、以及一定含有的离子。小组同学对上层溶液中还可能含有的离子进行了如下探究。
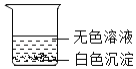
(提出问题)上层溶液中还可能含有什么离子?
(猜想与假设)上层溶液中还可能含有OH﹣、CO32﹣、Ca2+中的一种或几种。
(进行实验)
实验步骤 | 实验现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液 ②继续滴加稀盐酸 | ①溶液变红 ②产生气泡 | ①有OH﹣ ②有CO32﹣无Ca2+ |
方案二 | 取少量溶液于试管中,__(合理即可)(指示剂除外) | _(合理即可) | ①有CO32﹣,无Ca2+②有OH﹣ |
(反思与评价)
(1)小明同学对方案提出质疑,他的理由是___( 合理即可)。
(2)经过综合分析,最终确定上层溶液中肯定存在的离子有___。
(3)将烧杯内物质过滤,滤渣回收,向滤液中加入适量__( 合理即可)进行处理后再排放。