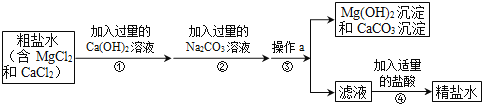
题目内容
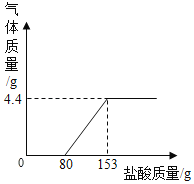
【题目】现有一包Na2CO3和NaOH固体样品,为了测定Na2CO3的质量分数,取该样品20g,加水搅拌至全部溶解.然后逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示。请计算:
(1)生成气体的质量____;
(2)该样品中Na2CO3的质量分数____;
(3)所用稀盐酸溶质的质量分数____.
【答案】4.4g 53% 10%
【解析】
根据给出的图可以看出生成了4.4g 二氧化碳,二氧化碳来自于碳酸钠和73g盐酸反应,所以根据二氧化碳的质量和对应的化学方程式求算碳酸钠和HCl的质量,进而求算对应的质量分数。
(1)由图可以看出碳酸钠和73g盐酸反应4.4g二氧化碳.
(2)设碳酸钠的质量为x,HCl的质量为y。
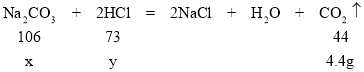
![]()
x=10.6g
y=7.3g
该样品中Na2CO3的质量分数为![]() ×100%=53%;
×100%=53%;
(3)所用稀盐酸溶质的质量分数为![]() ×100%=10%.
×100%=10%.
答:(1)生成气体的质量为4.4g;
(2)该样品中Na2CO3的质量分数为53%;
(3)所用稀盐酸溶质的质量分数为10%.

练习册系列答案
相关题目