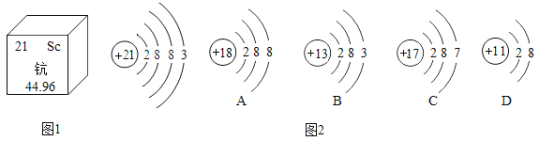
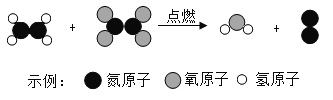
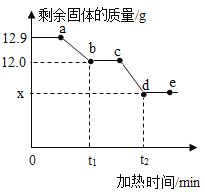
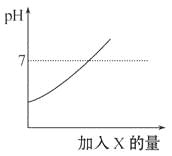
��Ŀ����
����Ŀ����ѧʵ����̾�������������ķ�Һ������������������Ч��ֹˮ����Ⱦ����һ��ʵ����ϣ���ȤС���ͬѧ�������NaOH��Һ��Na2CO3��Һ�ļ��𣬲��Է�Һ�ɷ�չ��̽����
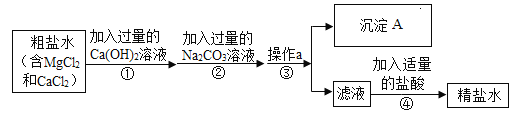
�һ ͨ��С�������ͬѧ���������ͼ��ʾ������Сʵ�顣ʵ�������ɰ�ɫ�����Ļ�ѧ����ʽ��_��дһ������
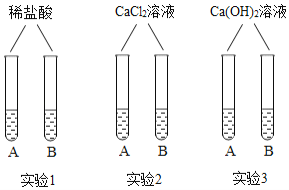
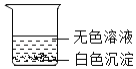
��� Сѩ����֧�Թ��е�ʣ���ﵹ��һ���ྻ�Ĵ��ձ��У���ͼ������ֽ��衢���ã��۲쵽�����ϲ�����ɫ��Һ���²��а�ɫ�������ɴ˿���ȷ�����ϲ���Һ��һ�������е�������_���Լ�һ�����е����ӡ�С��ͬѧ���ϲ���Һ�л����ܺ��е����ӽ���������̽����
��������⣩�ϲ���Һ�л����ܺ���ʲô���ӣ�
����������裩�ϲ���Һ�л����ܺ���OH����CO32����Ca2+�е�һ�ֻ��֡�
������ʵ�飩
ʵ�鲽�� | ʵ������ | ʵ����� | |
����һ | ��ȡ������Һ���Թ��У��μ���ɫ��̪��Һ �ڼ����μ�ϡ���� | ����Һ��� �ڲ������� | ����OH�� ����CO32����Ca2+ |
������ | ȡ������Һ���Թ��У�__���������ɣ���ָʾ�����⣩ | _���������ɣ� | ����CO32������Ca2+����OH�� |
����˼�����ۣ�
��1��С��ͬѧ�Է���������ɣ�����������___�� �������ɣ���
��2�������ۺϷ���������ȷ���ϲ���Һ�п϶����ڵ�������___��
��3�����ձ������ʹ��ˣ��������գ�����Һ�м�������__�� �������ɣ����д��������ŷš�
���𰸡�Na2CO3+CaCl2�TCaCO3��+2NaCl ������ �μ�ϡ���� ������������������� ̼������Һ�Լ��ԣ�Ҳ��ʹ��̪��Һ���ɫ �����ӡ������ӡ����������ӡ�̼������� ϡ����
��������
�һ���Ȼ�����̼���Ʒ�Ӧ�������ɫ�������˷�Ӧ�Ļ�ѧ����ʽΪ��Na2CO3+CaCl2�TCaCO3��+2NaCl��
�����Сѩ����֧�Թ��е�ʣ���ﵹ��һ���ྻ�Ĵ��ձ��У���ֽ��衢���ã��۲쵽�����ϲ�����ɫ��Һ���²��а�ɫ�������ɴ˿���ȷ�����ϲ���Һ��һ�������е������������ӣ��������ӹ���ԭ��֪����ɫ����Ϊ̼��ƣ�����Һ���������Ӵ��ڣ���̼����������Ӳ����棬������Һ��һ��û�������ӣ�
��������ʵ������Ǣ���CO32������Ca2+����OH��������Ӧ����Һ�еμ�ϡ���ᣬ��ϡ�����е��������������������ӷ�Ӧ����ˮ������̼������ӷ�Ӧ����������̼������ʵ���������������������������ݣ�
[��˼������]
��1��С��ͬѧ�Է���������ɣ�����������̼������Һ�Լ��ԣ�Ҳ��ʹ��̪��Һ���ɫ��
��2�������ۺϷ����������ӡ������������������ӹ��棬�ֲ�����������������ӣ���������ȷ���ϲ���Һ�п϶����ڵ������������ӡ������ӡ����������ӡ�̼������ӡ�
��3�����ձ������ʹ��ˣ��������գ�����Һ����̼������Ӻ����������ӣ���������Һ�м�������ϡ������д��������ŷš�
�ʴ�Ϊ(1). Na2CO3+CaCl2�TCaCO3��+2NaCl (2). ������ (3). �μ�ϡ���� (4). ������������������� (5). ̼������Һ�Լ��ԣ�Ҳ��ʹ��̪��Һ���ɫ (6). �����ӡ������ӡ����������ӡ�̼������� (7). ϡ����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���±����Ȼ��ƺ�������ڲ�ͬ�¶�ʱ���ܽ�ȡ�
�¶�/�� | 20 | 40 | 60 | 80 | |
�ܽ��/g | �Ȼ��� | 36.0 | 36.6 | 37.3 | 38.4 |
����� | 31.6 | 63.9 | 110.0 | 169.0 | |
��1�����������У��ܽ�ȵı仯���¶�Ӱ���С����_____��
��2��20��ʱ��100gˮ�м���25g�Ȼ��Ƴ���ܽ⣬������Һ�����ʵ���������Ϊ_____��
��3��ʹ�ӽ����͵��������Һ��Ϊ������Һ��һ�ַ�����_____��
��4��60��ʱ������ر�����Һ�����������Ȼ��ƣ��ᴿ����صķ�����_____��