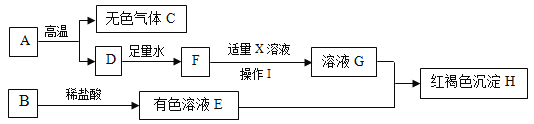
【题目】某化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
(提出问题)澄清石灰水为什么没有变浑浊?
(查阅资料)(1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2。
(2)AgCl不溶于稀硝酸
(提出猜想)Ⅰ.石灰水已完全变质 Ⅱ.___________ Ⅲ.CO2中混有HCl
(实验方案)兴趣小组用原药品继续制取CO2,并进行探究。
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 取少量澄清石灰水于试管中,加入______溶液。 | 产生白色沉淀。 | 猜想Ⅰ不成立。 |
(2) | 将少量气体通入盛有澄清石灰水的试管中。 | ______。 | 猜想Ⅱ不成立。 |
(3) | 将气体通入盛有____溶液的试管中,再加稀硝酸。 | ______。 | 猜想Ⅲ成立。反应方程式为____。 |
(实验结论)制取的气体CO2中混入了HCl,所以澄清石灰水没有变浑浊。
(交流讨论)若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和____。
(拓展思考)回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是_____(写一点)。
【题目】制作糕点常用 Na2CO3或 NaHCO3 作膨松剂,我校化学兴趣小组的同学根据 Na2CO3 和 NaHCO3的性质进行了一系列探究。
(查阅资料)
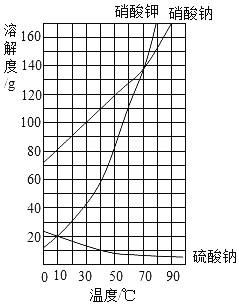
(1)溶解度比较:
溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(2)已知碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解。
(探究一)NaHCO3 和Na2CO3 溶解度差异的探究。
小方同学分别取 xg 两种固体粉末加入 20℃10 g 水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x 可能是_________________。
A 2 B 0.96 C 0.5 D 3
(探究二)测定某 Na2CO3和NaHCO3混合物中 NaHCO3的质量分数
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:_________________;
(2)实验中,需加热至恒重的目的是_________________。
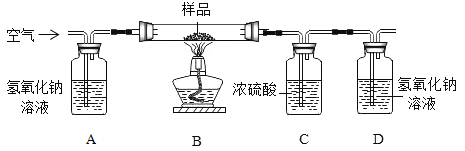
[方案二]利用下图装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量)。
(实验步骤)
(1)检查装置的气密性; (2)称取样品 10 g,加到装置 B 中; (3)称量装置 B、C、D 的质量(含药品);(4) 连接装置; (5)加热;(6)停止加热继续通入空气;(7)再次称量装置 B、C、D 的质量(含药品)。
(数据记录)
装置B | 装置C | 装置D | |
实验前物质的质量/g | 180.0 | 200.0 | |
试验后物质的质量/g | 176.9 | 201.5 | 124.8 |
(问题回答)
①上图装置 C 的作用是_________________,装置 C 中一个明显的错误是_________________。
②实验过程中必须向装置内通入空气,装置 A 中发生的化学方程式为_________________,若没有装置 A,造成测定结果_________________ (填“偏大”“不变”或“偏小”)。
(讨论分析)
小红同学认为,表格中三组数据都可以计算该样品中 NaHCO3的质量分数,但小张认为不能用 C 装置的质量变化来计算,其理由是_________________;改进方法:_________________;小王又认为用装置 D 的质量差会偏大而影响计算,应增加一个操作:_________________,目的是_________________。
(数据处理)经过反复讨论,大家一致赞成应该利用表格中的装置 B 的质量变化进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数_________________。
(拓展应用)固体Na2CO3中混有少量NaHCO3,可通过_________________方法除去。