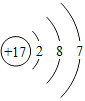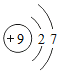题目内容
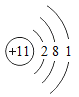
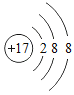
【题目】欲测定Cu-Zn合金及Cu-Ag合金中铜的质量分数,实验室只提供一瓶未标明质量分数的稀硫酸和必要的仪器。
(1)你认为能测出铜的质量分数的是 合金;
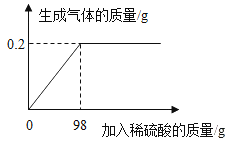
(2)取该合金的粉末26g加入该硫酸充分反应,所加稀硫酸与生成气体的质量关系如图所示,则:
①生成气体的质量为 g;
②请计算:合金与酸恰好完全反应时所得溶液的溶质质量分数。(写出计算过程,结果保留至0.1%)
【答案】(1)Cu-Zn;(2)①0.2;②15.4%
【解析】
(1)由于铜和银均不与和稀硫酸反应,只有锌能与稀硫酸反应,故只能测定铜锌合金中铜的质量分数;
(2)①由图像可知,生成的氢气的质量为0.2g;
②设锌的质量为x,生成的硫酸锌的质量为y;
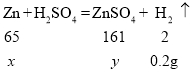
![]()
![]()
x=6.5g;y=16.1g
合金与酸恰好完全反应时所得溶液的溶质质量分数为![]() 。
。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案【题目】某兴趣小组的同学在做完酸、碱、盐相关性质的实验后,把稀盐酸、氢氧化钾溶液和碳酸钾溶液混合在一起,观察到有大量气泡产生,他们对反应后溶液中溶质的成分感到好奇并进行实验探究。
(查阅资料)碳酸钾溶液呈碱性。
(提出问题)反应后溶液中溶质的成分是什么?
(做出猜想)猜想①:KCl、K2CO3;猜想②:KCl、HCl;猜想③:KCl;猜想④:KCl、HCl、K2CO3;猜想⑤:KCl、K2CO3、KOH。
上述猜想中,你认为不合理的是猜想_____(填序号),理由是_____;
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
Ⅰ、取少量反应后的溶液于试管中,向其中加入过量的BaCl2溶液,充分反应后过滤 | _____ | 猜想②、③不成立 |
Ⅱ、取步骤Ⅰ后的上层清液,向其中滴加无色酚酞溶液 | _____ | 猜想⑤成立 |
(拓展应用)
(1)写出实验步骤Ⅰ中发生反应的化学方程式:_____;
(2)在确定化学反应后所得液体的溶质成分时,除了考虑生成物外,还要考虑_____。
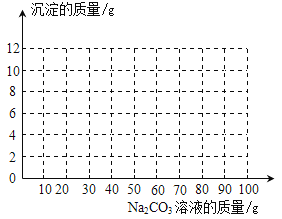
【题目】将 20g由NaCl和CaCl2组成的固体混合物,溶于水配成50g溶液, 向所得到的混合溶液中逐滴加入一定质量分数的Na2CO3溶液,加入Na2CO3溶液的质量与所得沉淀的质量关系如下表:
Na2CO3溶液的质量/g | 2 0 | 4 0 | 6 0 | 8 0 | 1 0 0 |
生成沉淀的质量/g | 4 | 8 | x | 10 | 10 |
(1)x的值为 。
(2)求所加Na2CO3 溶液中溶质的质量分数(写出计算过程)。
(3)画出产生沉淀与所加Na2CO3溶液质量关系的曲线图。
【题目】制作糕点常用 Na2CO3或 NaHCO3 作膨松剂,我校化学兴趣小组的同学根据 Na2CO3 和 NaHCO3的性质进行了一系列探究。
(查阅资料)
(1)溶解度比较:
溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(2)已知碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解。
(探究一)NaHCO3 和Na2CO3 溶解度差异的探究。
小方同学分别取 xg 两种固体粉末加入 20℃10 g 水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x 可能是_________________。
A 2 B 0.96 C 0.5 D 3
(探究二)测定某 Na2CO3和NaHCO3混合物中 NaHCO3的质量分数
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:_________________;
(2)实验中,需加热至恒重的目的是_________________。
[方案二]利用下图装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量)。
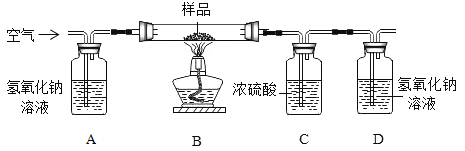
(实验步骤)
(1)检查装置的气密性; (2)称取样品 10 g,加到装置 B 中; (3)称量装置 B、C、D 的质量(含药品);(4) 连接装置; (5)加热;(6)停止加热继续通入空气;(7)再次称量装置 B、C、D 的质量(含药品)。
(数据记录)
装置B | 装置C | 装置D | |
实验前物质的质量/g | 180.0 | 200.0 | |
试验后物质的质量/g | 176.9 | 201.5 | 124.8 |
(问题回答)
①上图装置 C 的作用是_________________,装置 C 中一个明显的错误是_________________。
②实验过程中必须向装置内通入空气,装置 A 中发生的化学方程式为_________________,若没有装置 A,造成测定结果_________________ (填“偏大”“不变”或“偏小”)。
(讨论分析)
小红同学认为,表格中三组数据都可以计算该样品中 NaHCO3的质量分数,但小张认为不能用 C 装置的质量变化来计算,其理由是_________________;改进方法:_________________;小王又认为用装置 D 的质量差会偏大而影响计算,应增加一个操作:_________________,目的是_________________。
(数据处理)经过反复讨论,大家一致赞成应该利用表格中的装置 B 的质量变化进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数_________________。
(拓展应用)固体Na2CO3中混有少量NaHCO3,可通过_________________方法除去。
【题目】小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体展开探究,请你与他们一起进行探究.
【提出问题】这瓶氢氧化钠固体是否变质?
【查阅资料】CaCl2溶液呈中性.
【猜想与假设】①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠 .
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
实验步骤 | 实验现象 | 结论及解释 |
(1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想 不成立 |
(2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生 | 反应的化学方程式为: |
(3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想 成立 |
【反思与交流】久置的氢氧化钠变质的原因是(用化学方程式表示) ,因此,氢氧化钠应 保存.
【探索与拓展】为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为114.2g.试计算:
(1)该样品中碳酸钠的质量为 ;
(2)该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数)为 .