题目内容
【题目】如图所示是三种物质的溶解度曲线。请回答:

(1)溶解度随温度升高而降低的是_______;30℃时溶解度最大的是____。
(2)80℃时硝酸钠饱和溶液的溶质质量分数为____。使硝酸钠不饱和溶液变为饱和溶液,可采取的措施有_______(写一种)。
(3)某硝酸钾固体中混有少量硫酸钠杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、______、过滤、洗涤、干燥。
(4)30℃用等质量的硝酸钾、硝酸钠配制两种物质的饱和溶液需要水的质量硝酸钾____硝酸钠(填“>”“<”或“=”);
(5)配制一定溶质质量分数的硝酸钾溶液,以下操作中会导致所配制溶液溶质质量分数偏低的是____。
A 量筒量取水时仰视读数
B 配制好的溶液向细口瓶转移时溅出
C 硝酸钾固体中含有杂质
D 烧杯事先用水润洗过,内壁有水
【答案】硫酸钠 硝酸钠 60% 加硝酸钠或降温或恒温蒸发水 降温结晶 > ACD
【解析】
(1)由溶解度曲线可知:溶解度随温度升高而降低的是硫酸钠;30℃溶解度最大的是硝酸钠;
(2)80℃时硝酸钠的溶解度是150g,饱和溶液的溶质质量分数=![]() ;硝酸钠的溶解度随温度升高而增大,使硝酸钠不饱和溶液变为饱和溶液,可采取的措施有:增加溶质、降低温度或减少溶剂;故答案为:60%;加硝酸钠或降温或恒温蒸发水;
;硝酸钠的溶解度随温度升高而增大,使硝酸钠不饱和溶液变为饱和溶液,可采取的措施有:增加溶质、降低温度或减少溶剂;故答案为:60%;加硝酸钠或降温或恒温蒸发水;
(3)硝酸钾的溶解度随温度升高而增大,且变化较大,某硝酸钾固体中混有少量硫酸钠杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、降温结晶、过滤、洗涤、干燥;故答案为:降温结晶;
(4)30℃时硝酸钾的溶解度小于硝酸钠,用等质量的硝酸钾、硝酸钠配制两种物质的饱和溶液硝酸钾需要水的质量大于硝酸钠,故填“>”;
(5) A、量筒量取水时仰视读数,会导致量取的水体积偏大,溶质质量分数偏低,故正确;
B、配制好的溶液浓度不再改变,向细口瓶转移时溅出不会影响质量分数,故错误;
C、硝酸钾固体中含有杂质,溶质硝酸钾质量偏小,溶液溶质质量分数偏低,故正确;
D、烧杯事先用水润洗过,内壁有水,溶剂质量偏大,溶质质量分数偏低,故正确。
故选ACD。

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
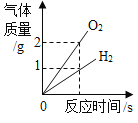
单元期中期末卷系列答案【题目】如图表示某个化学反应,据图分析判断,下列各项中,不正确的是( )

A. 该反应属于置换反应.
B. 反应中乙、丙两物质质量比为2: 7
C. 图示中x的数值为4
D. 反应前后氢元素的化合价发生了改变
【题目】某校化学兴趣小组的同学在实验室整理化学药品时,发现一瓶金属铬。为了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,他们进行了如下探究活动。
[查阅资料]铬(Cr)是银白色金属,在空气中表面能形成致密的氧化膜
[提出假设]考虑到铝的活动性比铜强,提出了三种假设:
假设①:A1>Cr>Cu
假设②:______。
假设③:____。
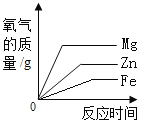
[实验过程]取大小相同的Cr、Cu、Al三种金属薄片,用砂纸打磨光亮后,分别放入三支试管中,再分别加入等体积20%的稀硫酸。
[实验现象]
金属 | Cr | Cu | Al |
实验现象 | 铬片表面产生气泡缓慢 | 铜表面无明显变化 | 铝表面产生 气泡较快 |
[实验结论]假设____成立(填序号)。
[问题与反思]
(1)由上述结论可知:铬可以与硫酸铜溶液发生反应。请写出该反应的化学方程式:____(已知在该反应的生成物中铬元素显+2价)。
(2)小丽提出,按上述实验操作,用硫酸铜溶液代替稀硫酸也能得出三种金属的活动性顺序,你认为____(填“可行 ”或“不可行”),理由是____。