题目内容
【题目】某化学兴趣小组在探究物质燃烧条件时,做了如下实验:
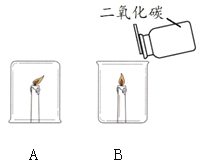
同学们发现两支蜡烛都熄灭了。
(提出问题)实验A中蜡烛熄灭的原因是什么?
(猜想与假设)
猜想1:烧杯内的氧气被耗尽,所以蜡烛熄灭。
猜想2:烧杯内的二氧化碳含量升高,所以蜡烛熄灭。
(进行实验)
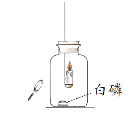
实验I:点燃蜡烛,塞紧胶塞。待蜡烛熄灭后,用放大镜照射白磷。观察到白磷燃烧。
实验II:经检测,实验A中,蜡烛熄灭时,烧杯内二氧化碳的体积分数约为3%。在集气瓶中按照一定的体积比收集气体,分别放入燃烧的蜡烛和燃烧的红磷,实验记录如下:
V(O2):V(CO2) | 蜡烛 | 红磷 |
1:4 | 燃烧 | 燃烧 |
1:5 | 燃烧 | 燃烧 |
1:6 | 熄灭 | 燃烧 |
1:9 | 熄灭 | 燃烧 |
(解释与结论)
(1)实验B中蜡烛熄灭,体现二氧化碳的化学性质是_______。
(2)实验I的目的是_______。
(3)写出红磷燃烧的化学方程式_______。
(4)实验II证明猜想2错误,依据的实验现象是_______。
(5)结合实验I与实验II,得出的实验结论是_______。
(实验反思)
(6)通过此实验,同学们对物质燃烧的条件有了新的认识,如_______。
【答案】不可燃,不助燃 验证猜想1是否正确(其他答案合理即可) 4P+5O2 ![]() 2P2O5 V(O2):V(CO2)=1:4或1:5时,蜡烛仍能燃烧 实验A中蜡烛熄灭是因为烧杯内氧气浓度降低,不足以支持蜡烛燃烧 不同可燃物燃烧所需的最低氧气浓度可能不同(其他答案合理即可)
2P2O5 V(O2):V(CO2)=1:4或1:5时,蜡烛仍能燃烧 实验A中蜡烛熄灭是因为烧杯内氧气浓度降低,不足以支持蜡烛燃烧 不同可燃物燃烧所需的最低氧气浓度可能不同(其他答案合理即可)
【解析】
根据已有的知识进行分析,二氧化碳的密度比空气大,当温度高时,二氧化碳的密度会减小,二氧化碳既不燃烧也不支持燃烧。
(1)实验B中蜡烛熄灭,体现二氧化碳的化学性质是不可燃,不助燃;
(2)验证猜想1是否正确(其他答案合理即可);
(3)红磷燃烧生成五氧化二磷,反应的化学方程式为4P+5O2![]() 2P2O5;
2P2O5;
(4)实验II证明猜想2错误,依据的实验现象是V(O2):V(CO2)=1:4或1:5时,蜡烛仍能燃烧;
(5)结合实验I与实验II,得出的实验结论是实验A中蜡烛熄灭是因为烧杯内氧气浓度降低,不足以支持蜡烛燃烧;
(6)通过此实验,同学们对物质燃烧的条件有了新的认识,如不同可燃物燃烧所需的最低氧气浓度可能不同(其他答案合理即可)。

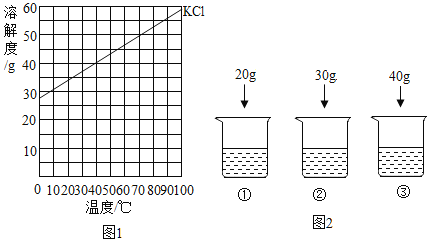
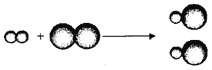
【题目】实验小组同学做了如下实验,验证质量守恒定律。
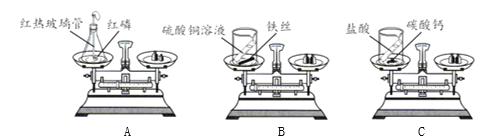
(1)实验A中发生反应的化学方程式为_______。
(2)上述实验中,不能用于验证质量守恒定律的是______(填实验序号),其原因是______。
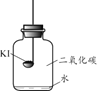
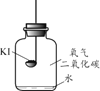
【题目】碘化钾(KI)保存不当会变质。实验小组进行以下实验探究KI变质的因素。
(提出问题1) KI变质的条件是什么?
(查阅资料)
① KI为白色粉末,暴露在空气中或久置会被氧化为碘(I2)而泛黄变质。
② 碘水中含较多KI时,滴加淀粉溶液显紫色或蓝紫色
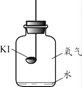
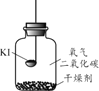
(进行实验)分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
实验1 | 实验2 | 实验3 | 实验4 |
|
|
|
|
固体变潮、表面变微黄 | 固体无明显现象 | 固体变潮、无其他明显现象 | 固体变潮、表面变黄 |
继续实验:取实验1中少量微黄固体溶解,加入淀粉溶液,溶液变紫色。
取实验4中少量黄色固体溶解,加入淀粉溶液,溶液变紫色。
(解释与结论)
(1)实验3的目的是_______。
(2)对比实验_______,可以得出KI变质一定与水有关。
(3)从上述实验可推知,KI变质的条件是_______。
(4)CO2的作用是______。