题目内容
【题目】某校兴趣小组对实验室一瓶敞口放置的氢氧化钠固体的变质程度进行探究:
(查阅资料)
①标准状况下,二氧化碳的密度p=1.977g/L
②碳酸钠与氯化钙反应的方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl
(设计实验)
方案一:气体分析法
(1)如下图所示,把Xg氢氧化钠样品与足量稀硫酸反应,通过测定二氧化碳的体积或质量计算出碳酸钠质量,从而计算出样品中碳酸钠或氢氧化钠的质量分数。检查图1装置气密性的方法是______。
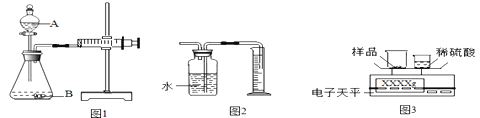
(2)甲同学用图1装置测量二氧化碳气体的体积,将二氧化碳的体积换算质量,进行计算。乙同学认为注射器中收集的气体体积会比反应产生的二氧化碳气体体积的准确值偏大,原因是______。
(3)乙同学提出用图2装置代替图1中的收集装置,测量生成二氧化碳的体积。丙同学认为所测得CO2的体积会比反应生成二氧化碳的准确值偏小,原因是____,为了防止因此产生的误差,你改进的方法是______。
(4)丙同学用图3装置测量生成CO2的质量。先记录反应前电子秤的示数,将足量的稀硫酸慢慢全部加入到大烧杯中,反应停止后,称量小烧杯和大烧杯及其内部剩余物质的总质量。丁同学认为所测结果与准确值比会偏大,原因是______。
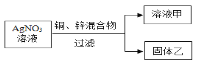
方案二:沉淀分析法
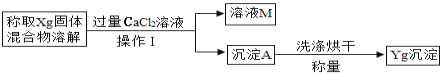
(1)“操作I”中用到的玻璃仪器有玻璃棒、烧杯和_______。
(2)如果沉淀A没有经过洗涤,就直接烘干称量,则导致测得的样品中氢氧化钠的质量分数_______(填“偏大”、“偏小”或“不变”)。
【答案】连接装置,推拉注射器活塞,如果活塞回到原处,说明装置不漏气 流下的稀硫酸占据一定体积 二氧化碳能够溶于水 在水面上覆盖一层植物油 部分水蒸气随着二氧化碳逸出 漏斗 偏小
【解析】
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳,二氧化碳能够溶于水,不溶于植物油;氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,根据反应的化学方程式及其提供的数据可以计算碳酸钠质量,进一步可以计算氢氧化钠质量及其碳酸钠、氢氧化钠的质量分数。
方案一:(1)检查图1装置气密性的方法是:连接装置,推拉注射器活塞,如果活塞回到原处,说明装置不漏气;
(2)注射器中收集的气体体积会比反应产生的二氧化碳气体体积的准确值偏大,原因是流下的稀硫酸占据一定体积;
(3)丙同学认为所测得CO2的体积会比反应生成二氧化碳的准确值偏小,原因是二氧化碳能够溶于水,为了防止因此产生的误差,改进的方法是:在水面上覆盖一层植物油;
(4)丁同学认为所测结果与准确值比会偏大,原因是部分水蒸气随着二氧化碳逸出;
方案二:(1)“操作 I”是过滤,用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)如果沉淀A没有经过洗涤,就直接烘干称量,会导致碳酸钙质量偏大,从而导致碳酸钠质量偏大,进一步导致氢氧化钠质量偏小,则导致测得的样品中氢氧化钠的质量分数偏小。

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案【题目】某实验小组利用废硫酸液制备K2SO4

(1)将CaCO3研成粉末的目的是 .
(2)上述流程中可循环使用的物质有CO2和 (填写化学式).
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入 (选填序号,下同),振荡、静置,再向上层清液中滴加 ,观察现象即可判断.
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
【题目】元素周期表是学习化学的重要工具。下表是元素周期表的一部分,请回答下列问题:
1H | 2He | ||||||
3Li | 4Be | 5B | 6C | 7N | 8O | 9F | 10Ne |
11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar |
(1)元素周期表中不同种元素最本质的区别是______(填字母)。
A.相对原子质量不同 B.质子数不同 C.中子数不同
(2)镁元素的原子结构示意图为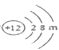 ,则m=______,该原子在化学反应中易______(填“得到”或“失去”)电子,说明元素的化学性质与原子的______关系密切。
,则m=______,该原子在化学反应中易______(填“得到”或“失去”)电子,说明元素的化学性质与原子的______关系密切。
【题目】钙元素对人类生命和生活具有重要意义,含钙的物质是中学化学研究的重要内容。
(1)牛奶中的钙主要以磷酸钙(Ca3(PO4)2 的形式存在,磷酸钙中磷元素的化合价为_____价。
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是_____(填“吸热”或“放热”)。
(3)氢化钙固体是登山运动员常用的能源提供剂某研究小组的同学通过查阅资料得知:氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。该研究小组的同学把一定量的氢化钙加入到碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
(提出问题)滤液中溶质的成分是什么?
猜想一:氢氧化钠
猜想二:氢氧化钠、氢氧化钙
猜想三:氢氧化钠、碳酸钠
猜想四:氢氧化钠、碳酸钠、氢氧化钙
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明理由_____。
(实验验证)
实验 | 现象 | 结论 |
①取少量滤液,向其中滴加少量碳酸钠溶液 | 无明显现象 | 猜想_____不成立 |
②另取少量滤液,向其中滴加足量稀盐酸 | _____ | 猜想三成立 |
(反思与拓展)
①要证明猜想三成立,也可以另取少量滤液,向其中滴加_____。
②在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑_____。
③登山运动员携带氢化钙作为能源提供剂与携带氢气相比,其优点是_____(写一条即可)。