题目内容
【题目】金属材料在日常生活中已得到越来越广泛的应用。
(1)钢铁部物件一般要进行喷漆等处理,以防止其生锈,铁生锈的实质是铁与空气中的氧气、_____等发生化学反应。
(2)设计实验验证锌、铜、银三种金属活动性强弱的方案有多种,其中可选用试剂锌片、银片和___(填化学式)溶液进行验证。
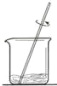
(3)如图,向一定量AgNO3溶液中加入一定量的铜、锌的混合物粉末,充分反应后过滤,得到溶液甲和固体乙。
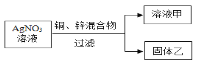
①若溶液甲为蓝色,则固体乙中可能含有的物质是____。
②若固体乙中含有锌、铜、银三种,则溶液甲中所含的金属离子符号为__________。
【答案】水 CuSO4(或CuCl2或Cu(NO3)2) 铜 Zn2+
【解析】
(1)对钢铁部件进行喷漆可以防止其生锈,铁生锈的实质是铁与空气中的氧气、水蒸气等发生化学反应;
(2)在金属活动顺序表中,金属的活动性顺序是锌>铜>银;设计实验验证锌、铜、银三种金属活动性强弱的方案有多种,其中可选用试剂锌片、银片和铜的盐溶液如硫酸铜、氯化铜、硝酸铜等,化学式为:CuSO4(或CuCl2或Cu(NO3)2);
(3)在金属活动顺序表中,金属的活动性顺序是锌>铜>银,向一定量AgNO3溶液中加入铜和锌的混合粉末时,锌先与硝酸银反应,当锌反应完后,铜再与硝酸银反应;
①若溶液甲显蓝色,说明了铜与硝酸银反应生成了硝酸铜,化学反应方程式为:Cu+2AgNO3═2Ag+Cu(NO3)2,此时固体乙中一定含有的物质是银,可能含有铜;
②若乙中含有锌、铜、银三种固体,说明了溶液中没有硝酸银、硝酸铜,则溶液甲中所含的金属离子符号为:Zn2+。

【题目】初中化学常见的3种元素X、Y和Z相关信息如下表所示
元素 | X | Y | Z |
相关信息 | 它的单质甲是一种清洁能源 | 地壳中含量最多的元素 | 它的一种单质乙是天然存在的最硬的物质 |
(1)甲的化学式是______,乙的名称是______
(2)ZY2可与Z的单质在高温条件下反应生成ZY,该反应的化学方程式是____________
(3)A、B、C是由上述3种元素中的一种或两种组成的单质或化合物,G由Ca、Y和Z三种元素组成。它们之间的转化关系如下图所示(“→”表示转化关系,部分反应物、生成物及反应条件已略去)
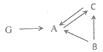
①G的化学式是________
②若A中不含X元素,则B的化学式为______C→A的化学方程式是________
③若A中不含Z元素,B→C的化学方程式是_________