题目内容
【题目】分析处理图表中的信息是学习化学的一种重要方法。运用溶解度表与溶解度曲线回答问题:
温度/°c | 0 | 10 | 20 | 30 | 40 | 50 |
NH4C1溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36,3 | 36. 6 | 37.0 |
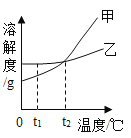
(1)氯化钠的溶解度曲线是_____(填"甲”或“乙”)。
(2)20℃时,将40 gNH4Cl加入100 g的水中,充分搅拌后得到的是______(填“饱和”或“不饱和”)溶液。将上述溶液升温到30 °C,该溶液的溶质质量分数为__
(3)t1 °C时,将甲、乙两种物质的饱和溶液各100 g分别恒温蒸发5 g水,析出晶体最多的是_____(填“甲”或'乙”)。
(4)计算配制50 g质量分数为3%的NaCl溶液所需质量分数为6%的NaCl溶液的体积,需要用到的数据是_____(填字母)。
A 3%的NaCl溶液的密度 B 水的密度 C 6%的NaCl溶液的密度
【答案】乙 饱和 28.6% 乙 C
【解析】
(1)由表格数据可知,氯化钠溶解度随温度升高变化不大,故选:乙;
(2)20℃时氯化铵溶解度37.2g,根据溶解度概念可知,40g氯化铵不能全部溶解形成饱和溶液,故填:饱和;
升高到30℃时,氯化铵全部溶解,溶质质量分数![]() ,故填:28.6%;
,故填:28.6%;
(3)t1 °C时根据溶度曲线可知乙溶解度大于甲溶解度,故相同质量水乙溶解的溶质多,蒸发相同质量水,乙结晶析出也多,故填:乙;
(4)配置50g3%氯化钠溶液需要6%氯化钠溶液质量为25g,溶液的质量等于溶液的体积乘以溶液的密度。现在要求6%氯化钠溶液质量我还需要知道6%氯化钠溶液的密度,故选C。

练习册系列答案
相关题目