题目内容
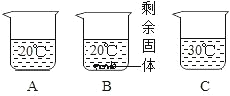
【题目】在20°C时,将等质量的A、B两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50°C时现象如图2,A、B两种物质的溶解度曲线如图3。试根据图示回答下列问题:
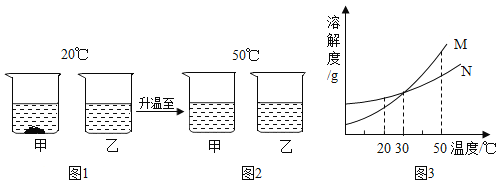
(1)图1中一定为饱和溶液的是__________。
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为____________(填“>”“<”或“=”)。
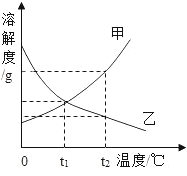
(3)图3中表示乙的溶解度曲线是____________。
【答案】甲 = N
【解析】
(1)饱和溶液是指在一定温度下,一定量的溶剂里不能再溶解某种溶质的溶液叫做这种溶质的饱和溶液;还能继续溶解某种溶质的溶液叫做这种溶质的不饱和溶液.
(2)溶质的质量分数=![]() 。
。
(3)根据图中信息可以知道20℃时甲的溶解度小于乙的溶解度,结合图3可以完成解答。
(1)从图1中可以知道甲中固体没有完全溶解,则说明甲中形成的溶液为饱和溶液;
(2)图2中相同质量的溶剂溶解了相同质量的溶质,所以它们形成溶液的质量也相等,结合溶质的质量分数=![]() 可以知道,它们形成的溶液中溶质的质量分数也相等;
可以知道,它们形成的溶液中溶质的质量分数也相等;
(3)根据图1中信息可以知道20℃时甲的溶解度小于乙的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故N表示的是乙物质的溶解度曲线。
故答案为:(1)甲;
(2)=;
(3)N。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】分析处理图表中的信息是学习化学的一种重要方法。运用溶解度表与溶解度曲线回答问题:
温度/°c | 0 | 10 | 20 | 30 | 40 | 50 |
NH4C1溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36,3 | 36. 6 | 37.0 |
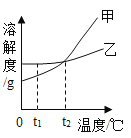
(1)氯化钠的溶解度曲线是_____(填"甲”或“乙”)。
(2)20℃时,将40 gNH4Cl加入100 g的水中,充分搅拌后得到的是______(填“饱和”或“不饱和”)溶液。将上述溶液升温到30 °C,该溶液的溶质质量分数为__
(3)t1 °C时,将甲、乙两种物质的饱和溶液各100 g分别恒温蒸发5 g水,析出晶体最多的是_____(填“甲”或'乙”)。
(4)计算配制50 g质量分数为3%的NaCl溶液所需质量分数为6%的NaCl溶液的体积,需要用到的数据是_____(填字母)。
A 3%的NaCl溶液的密度 B 水的密度 C 6%的NaCl溶液的密度