题目内容
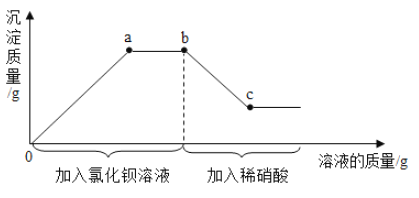
【题目】某溶液中可能含有碳酸钠、硫酸钠中的一种或两种溶质,为测定其成分,进行如下实验:取一定量溶液于烧杯中,先加入过量氯化钡溶液,再加入稀硝酸,反应过程及产生沉淀的质量与所加溶液质量的关系如图所示。下列说法中不正确的是
A. 该溶液中一定含有碳酸钠和硫酸钠
B. 反应进行到![]() 点时,溶液中只含有一种溶质
点时,溶液中只含有一种溶质
C. ![]() 段上的任意一点(
段上的任意一点(![]() 点除外)都存在的两种沉淀
点除外)都存在的两种沉淀
D. 反应进行到![]() 点时,溶液中只含有两种溶质
点时,溶液中只含有两种溶质
【答案】D
【解析】
A、由图中信息可知,加入稀硝酸后沉淀部分溶解,说明沉淀是碳酸钡和硫酸钡的混合物,因此该溶液中一定含有碳酸钠和硫酸钠,故不符合题意;
B、反应进行到a点时,碳酸钠、硫酸钠恰好和氯化钡完全反应,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,硫酸钠和氯化钡反应生成硫酸钡沉淀和氯化钠,溶液中只含有氯化钠一种溶质,故不符合题意;
C、![]() 段是碳酸钡和稀硝酸反应生成硝酸钡和水和二氧化碳,硫酸钡难溶于水和稀硝酸,所以
段是碳酸钡和稀硝酸反应生成硝酸钡和水和二氧化碳,硫酸钡难溶于水和稀硝酸,所以![]() 段上的任意一点(
段上的任意一点(![]() 点除外)都存在不反应的硫酸钡和未反应完的碳酸钡两种沉淀,故不符合题意;
点除外)都存在不反应的硫酸钡和未反应完的碳酸钡两种沉淀,故不符合题意;
D、反应进行到![]() 点时,碳酸钡恰好和稀硝酸反应完全生成硝酸钡,溶液中的溶质有新生成的硝酸钡、过量的氯化钡、氯化钠(氯化钡和碳酸钠、硫酸钠反应生成的)三种,故不符合题意;
点时,碳酸钡恰好和稀硝酸反应完全生成硝酸钡,溶液中的溶质有新生成的硝酸钡、过量的氯化钡、氯化钠(氯化钡和碳酸钠、硫酸钠反应生成的)三种,故不符合题意;
故选D。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】分析处理图表中的信息是学习化学的一种重要方法。运用溶解度表与溶解度曲线回答问题:
温度/°c | 0 | 10 | 20 | 30 | 40 | 50 |
NH4C1溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36,3 | 36. 6 | 37.0 |
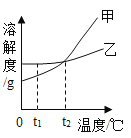
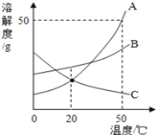
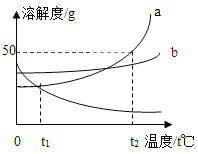
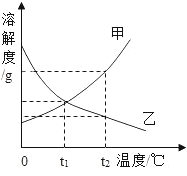
(1)氯化钠的溶解度曲线是_____(填"甲”或“乙”)。
(2)20℃时,将40 gNH4Cl加入100 g的水中,充分搅拌后得到的是______(填“饱和”或“不饱和”)溶液。将上述溶液升温到30 °C,该溶液的溶质质量分数为__
(3)t1 °C时,将甲、乙两种物质的饱和溶液各100 g分别恒温蒸发5 g水,析出晶体最多的是_____(填“甲”或'乙”)。
(4)计算配制50 g质量分数为3%的NaCl溶液所需质量分数为6%的NaCl溶液的体积,需要用到的数据是_____(填字母)。
A 3%的NaCl溶液的密度 B 水的密度 C 6%的NaCl溶液的密度