题目内容
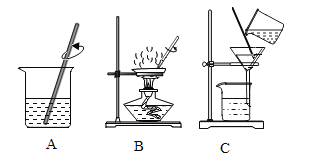
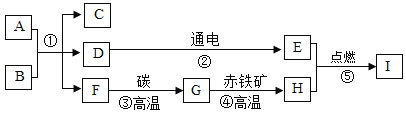
【题目】实验考试时,需要配用1%的氢氧化钠溶液100g,有关操作如图1所示;
(1)以上实验正确的操作顺序是_____(用字母代号表示),其中存在明显的错误操作是_____。
(2)量取一定体积的溶液时,需要选用的合适的仪器是_____。
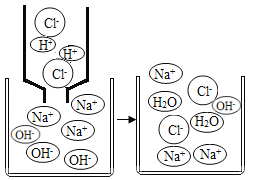
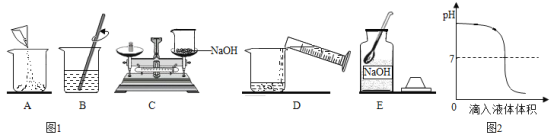
[实验拓展]如图2是氢氧化钠溶液和稀硫酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。滴加顺序有两种,a是将氢氧化钠溶液滴入硫酸中,b是将硫酸滴入氢氧化钠溶液中。根据曲线判断,该反应的滴加顺序是_____(填“a”或“b”)。
[实验反思]某同学在滴加过程中,意外发现了有气泡产生,请用化学方程式解释原因:_____(写一个即可)。
[实验结论]某已变质的氢氧化钠溶液100g, 向其中加入溶质质量分数9.8%的稀硫酸100g,恰好完全反应得到中性溶液。则蒸干该中性溶液可得到固体质量是_____。
【答案】ECADB C中物码倒置 量筒和胶头滴管 b ![]() 14.2克
14.2克
【解析】
(1)根据配制溶液的一般步骤:计算、称取、量筒、溶解、装瓶存放可知,其顺序为ECADB;由“左物右码”可知,C图中存在的错误是砝码与药品的位置颠倒了,应该是将盛有氢氧化钠固体的烧杯放在左盘上称量;故填:ECADB;C中物码倒置。
(2)量取一定体积的溶液时,需要用到量筒和胶头滴管;故填:量筒和胶头滴管。
[实验拓展]
根据图像,在反应未进行时,溶液的pH>7,为碱性溶液,所以该曲线反应是将盐酸滴入氢氧化钠溶液中;故填:b。
[实验反思]
氢氧化钠吸收空气中的二氧化碳会生成碳酸钠,碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳气体;故填:![]() 。
。
[实验结论]
无论是氢氧化钠还是碳酸钠与硫酸反应的生成物均有硫酸钠,恰好完全反应得到中性溶液,设生成硫酸钠的质量为x,则:

![]()
x=14.2g
故填:14.2克。

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案