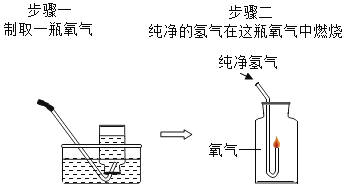
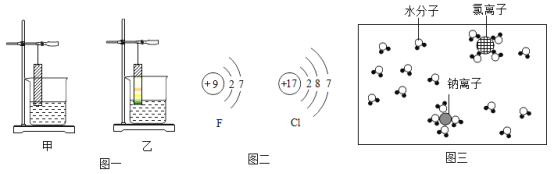
题目内容
【题目】A~I均为初中化学常见物质,它们之间的转化关系如下图,部分产物已略去。已知A是人体胃酸的主要成分,B是大理石的主要成分,D为液体,F为气体,I能与A反应生成个数比为1 : 2的+2价、+3价铁盐。
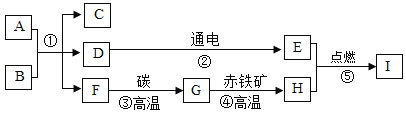
(1)写出下列物质的化学式:C_____________、H________________。
(2)上述①②③④⑤中属于化合反应的是_______________。
(3)写出G→H的化学反应方程式_______________。
(4)写出I和A反应的化学反应方程式_______________。
【答案】CaCl2 Fe ③⑤ 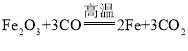
![]()
【解析】
A~I均为初中化学常见物质,A是人体胃酸的主要成分,可推出A是盐酸,B是大理石的主要成分,可推出B为碳酸钙,碳酸钙可与盐酸反应生成氯化钙、二氧化碳和水,F为气体,可推出F为二氧化碳,二氧化碳和碳能在高温的条件下反应生成一氧化碳,故G是一氧化碳,一氧化碳能与三氧化二铁在高温的条件下反应生成铁和二氧化碳,可推出H为铁,I能与盐酸反应生成个数比为1:2的+2价、+3价铁盐,可推出I为四氧化三铁,铁可在氧气中燃烧生成四氧化三铁,可推出E为氧气,水能在通电的情况下生成氧气,可推出D为水,则C为氯化钙。
(1)C为氯化钙,化学式为:CaCl2;H为铁,化学式为:Fe;
(2)反应①为碳酸钙与稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:![]() ,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;
,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;
反应②为水在通电的条件下分解为氢气和氧气,该反应的化学方程式为: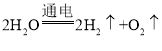 ,该反应符合“一变多”的特点,属于分解反应;
,该反应符合“一变多”的特点,属于分解反应;
反应③为二氧化碳与碳在高温的条件下生成一氧化碳,该反应的化学方程式为: ,该反应符合“多变一”的特点,属于化合反应;
,该反应符合“多变一”的特点,属于化合反应;
反应④为一氧化碳与三氧化二铁在高温的条件下反应生成铁和二氧化碳,该反应的化学方程式为: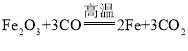 ,该反应不属于基本反应类型;
,该反应不属于基本反应类型;
反应⑤为铁在氧气中燃烧生成四氧化三铁,该反应的化学方程式为: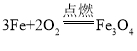 ,该反应符合“多变一”的特点,属于化合反应;
,该反应符合“多变一”的特点,属于化合反应;
故属于化合反应的是:③⑤;
(3)G为一氧化碳,H为铁,G→H的化学反应方程式为: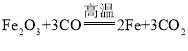 ;
;
(4)I能与A反应生成个数比为1:2的+2价、+3价铁盐,故四氧化三铁与稀盐酸反应生成氯化亚铁、氯化铁和水,该反应的化学方程式为:![]() 。
。

【题目】有一瓶标签受损、没盖瓶盖且装有无色液体的试剂瓶,如图所示。
老师告诉大家,瓶内原有的液体只能是碳酸钠溶液、氢氧化钠溶液、氯化钠溶液、蒸馏水中的一种。为了判断瓶内是何种溶质,并确定试剂瓶的标签,化学小组的同学进行了如下探究活动。
![]()
(实验探究)
(1)从受损的标签信息看,大家一致认为该液体不可能是___________。
(2)甲同学设计了如下方案进行探究。
实验操作 | 实验现象 | 实验结论 |
取适量瓶内液体加入试管中,滴加足量的稀盐酸 | ________ | 该液体是碳酸钠溶液 |
(3)乙同学认为甲同学的结论不准确,又设计了如下方案进行探究。
实验操作 | 实验现象 | 实验结论 |
取适量瓶内液体加入试管中,滴加过量Ca(OH)2溶液。静置后,取上层清液,滴加酚酞溶液 | ________ | 该液体中的溶质为氢氧化钠和碳酸钠。反应的化学方程式:________ |
(4)丙同学认为乙同学的实验方案有不足之处, 于是丙同学只改用了一种与乙同学所加物质类别不同的溶液,重新按照乙的方法进行实验,得到的实验现象和结论与乙同学的完全一致,且结论完全正确。则丙同学改用的试剂为_______________。
(实验结论)实验结束后,最终得到的结论是:原试剂瓶标签_____________。
(反思与交流)
(1)为了不使标签破损,应如何正确操作_______________________。
(2)药品取完之后应及时密封保存。
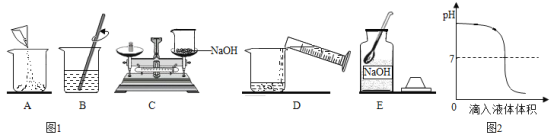
【题目】正确的方案设计和规范的实验操作有助于达到实验目的,请分析或改进以下实验。
实验目的 | 实验过程及现象 | 分析或改进 |
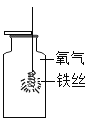
铁丝在氧气中燃烧 |
| 画图表示你的改进方法:_____。 |
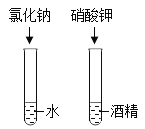
探究物质溶解性的影响因素 |
| 为达到实验目的,你的改进方法是_____。 |
通过氢气在氧气中燃烧证明水的组成 |
现象:氢气燃烧,发出_____色火焰, 瓶壁发热。 | 该实验不能达到实验目的的原因是_____。 |
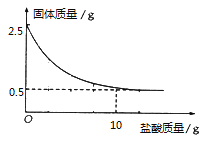
【题目】高铁的开通对丹东的发展起到极大的推动作用。高铁建设需要大量的钢铁材料.
(1)工业炼铁的原理方程式是_________(以赤铁矿为例)
(2)锰钢是一种合金,可用于高铁建设。已知金属活动性:锰>铁.锰的部分化合物溶解性见右表。若用实验验证铁、铜、锰三种金属的活动性,至少需要的三种试剂是_________
OH- | NO3- | Cl - | SO42- | CO32- | |
Mn2+ | 不 | 溶 | 溶 | 溶 | 不 |
(3)已知铁的硬度为5,锰的硬度为6,锰钢的硬度__(填“>6”、“<5”或“介于5-6之间”).
【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如右图),为确认其中的溶质,同学们进行了如下的探究活动。请你参与到其中去,回答有关问题。

【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想IV:该溶液的溶质是NaHCO3.
【查阅资料】常温下物质的相关信息如下表:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知,该溶液的溶质不是NaHCO3,因为常温下NaHCO3溶液溶质的质量分数最大是
(精确到01.%)。
【进行实验】
(1)测定溶液的pH大于7,该溶液的溶质不是 (填化学式)。
(2)同学们又进行了如下实验,实验过程如下:

①产生白色沉淀的化学方程式是 。
②实验可以判断原无色溶液中含有的溶质有 。
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且 (填“没有”、“部分”或“全部”)变质。
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的 ,然后过滤。反应化学方程式是 。