题目内容
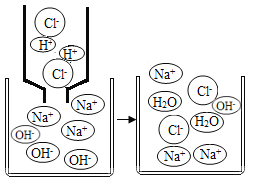
【题目】如图是氢氧化钠溶液与稀盐酸反应的微观示意图,请回答下列问题:
(1)酸和碱反应生成_____和水叫中和反应。
(2)反应后该溶液的pH_____7(填“>”、“<”或“=”),往溶液中滴加数滴酚酞试液,溶液_____。
(3)写出该反应的方程式:_____。
【答案】盐 > 变红 ![]()
【解析】
根据中和反应概念、反应后微观示意图以及稀盐酸与氢氧化钠反应生成氯化钠和水,进行分析解答。
(1)中和反应是酸与碱作用生成盐和水的反应,故填:盐。
(2)由反应后微观示意图,反应后的溶液中含有钠离子、氢氧根离子、氯离子和水分子,显碱性,该溶液的pH>7;酚酞遇碱变红,所以往溶液中滴加数滴酚酞试液,溶液变红,故填:>;变红。
(3)稀盐酸与氢氧化钠反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O。
故填:NaOH+HCl=NaCl+H2O。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】某实验小组的同学对“锌与硫酸反应速率的影响因素”进行探究,并利用如图装置收集产生的氢气。
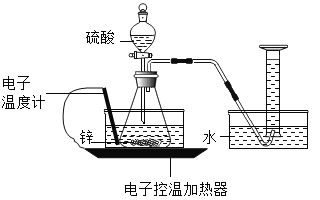
(查阅资料)
圆粒状锌的直径通常为 3-4 毫米,粉末状锌的直径通常为 0.3-0.5 毫米。
(进行实验)
实验 1:在不同温度下,进行锌与硫酸反应的实验。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
1-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
1-2 | 30 | 20 | 10% | 圆粒状 | 1 | 134 |
1-3 | 40 | 20 | 10% | 圆粒状 | 1 | 107 |
实验 2:在相同温度下,继续进行锌与硫酸反应速率的影响因素的探究。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
2-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
2-2 | 20 | 20 | 10% | 粉末状 | 1 | 47 |
2-3 | 20 | 20 | 20% | 圆粒状 | 1 | 88 |
2-4 | 20 | 20 | 20% | 粉末状 | 1 | 26 |
(解释与结论)
(1)锌与硫酸反应的化学方程式为_____ 。
(2)能用排水法收集氢气的原因是氢气_____(填“易”或“难”)溶于水。
(3)实验 1 的目的是_____。
(4)实验 2 中,欲得出“其他条件相同时,硫酸的溶质质量分数越大,锌与硫酸反应的速率越快”的结论,需要对比的实验_____(填编号)。
(5)实验 2 中,通过对比 2-1 和 2-2,得出的结论是_____。
(反思与评价)
(6)实验室制取氢气时,通常使用锌粒而不用锌粉的原因为_____。
(7)实验室中若使用 6.5g 锌粒制取氢气,理论上制得氢气的质量为_____g。