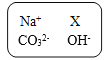题目内容
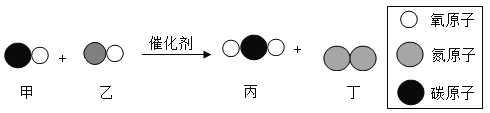
【题目】史书中,秦军战士被描绘成“左手拎人头,右手抓俘虏”的善战形象。秦军之所以能扫平六国,除了得益于制度和战略优势,还与精良的武器装备密不可分。 秦国的武器生产采取责任制,工匠要把名字刻在武器上 所以产品规格统一、质量过硬。在 上世纪 70 年代,人们甚至在检测兵马俑武器的化学成分时发现:有些武器的表面居然存在“含铬化合物” ,并推测秦人可能已经学会用含铬氧化层来防止兵器生锈。铬元素在元素周 期表中的信息如图所示,下列说法错误的是( )

A.铬原子中中子数为 28B.铬元素属于金属元素
C.铬元素相对原子质量为 52.00 gD.致密的铬氧化物层能防止兵器锈蚀
【答案】C
【解析】
A、铬原子中中子数为52-24=28,选项说法正确。
B、铬元素带金字旁,因此属于金属元素,选项说法正确。
C、铬元素相对原子质量为 52.00,单位不是“g”是“1”,省略不写,选项说法错误。
D、由题意可知,秦人可能已经学会用含铬氧化层来防止兵器生锈,因此致密的铬氧化物层能防止兵器锈蚀,选项说法正确。
故选:C。

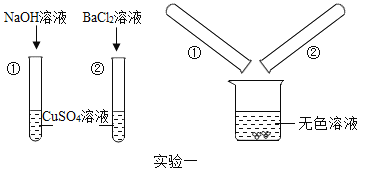
【题目】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了如图两个实验:
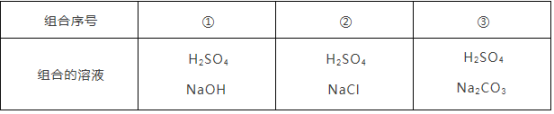
组合序号 | ① | ② | ③ |
组合的溶液 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 |
实验二
实验二
[实验一]:把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液
(1)写出混合后得到蓝色沉淀一定发生反应的化学方程式_____。
(2)混合后所得无色溶液中一定含有的溶质是_____(填化学式,下同)可能含有的溶质是_____。
[实验二]:
(3)在组合①、②、③中,组合_____无明显现象,但它们的实质不同,为了证明实质不同。小夕在实验过程中使用了酚酞试液
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。混合后所得溶液中除酚酞外溶质的组成可能是_____(填化学式)
[结论]:
(5)复分解反应发生的条件是:生成物中有_____。
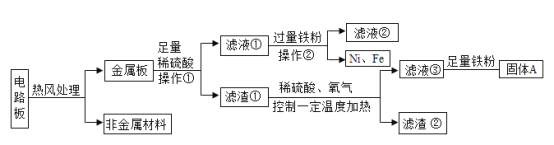
【题目】某校实验室有一瓶久置的铁粉,已部分锈蚀,某兴趣小组对其组成进行如下探究:
(1)定性探究:
取样品平铺于白纸上,用磁铁置于样品上方,黑色固体全部被吸起,白纸上留下______色固体;将被磁铁吸起的黑色固体全部投入硫酸铜溶液中,充分反应后,过滤,所得固体全部为红色。样品中含有铁和氧化铁。
(2)定量探究:
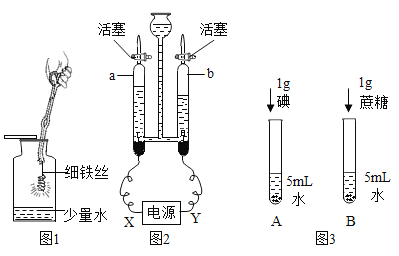
按下图所示装置进行实验(装置气密性良好,固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
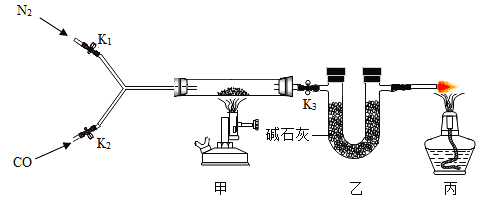
Ⅰ称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
Ⅱ连接好装置。缓缓通入N2,燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
数据如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤Ⅱ硬 质玻璃管和剩余固体 | 步骤Ⅲ硬质玻璃管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
①步骤Ⅲ丙处酒精灯的作用是_______。
②步骤Ⅲ玻璃管中反应的化学方程式为______。
③样品中氧化铁的质量分数为_______(用m1、m2、m3、m4的代数式表示)。
④若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将_____(填“偏大”“偏小”或“不变”)。
⑤有关样品,下列说法正确的是_____(填序号,多选)。
A样品中氢元素的质量为![]()
B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1
D样品中氧元素的质量为m3-m4
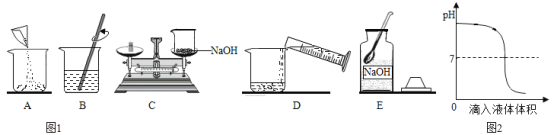
【题目】正确的方案设计和规范的实验操作有助于达到实验目的,请分析或改进以下实验。
实验目的 | 实验过程及现象 | 分析或改进 |
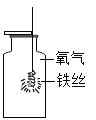
铁丝在氧气中燃烧 |
| 画图表示你的改进方法:_____。 |
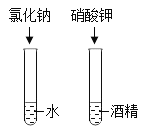
探究物质溶解性的影响因素 |
| 为达到实验目的,你的改进方法是_____。 |
通过氢气在氧气中燃烧证明水的组成 |
现象:氢气燃烧,发出_____色火焰, 瓶壁发热。 | 该实验不能达到实验目的的原因是_____。 |