题目内容
某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合.加热该混合物t1时间后(杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
(1)加热t3时间后氯酸钾是否已经完全反应? (填是或否).
(2)求完全反应后产生氧气的质量 .
(3)求该样品中氯酸钾的质量分数.
(1)是(2)0.96g
(3)设样品中氯酸钾的质量为X。
根据化学方程式可知 245:96=X:0.96g
X=2.45g
所以该样品中氯酸钾的质量分数为 2.45g/2.5g=98%
解析试题分析:本题是一道数据分析式的计算题,把质量守恒定律与化学方程式的计算相结合。首先样品2.5g和0.5g二氧化锰一共是3g,加热到时继续加热,固体质量不再变化,说明此时样品中的氯酸钾已经完全分解,得到的氧气质量为2.45g+0.5g-2.04g=0.96g,然后根据化学方程式用氧气的质量求出氯酸钾的质量,从而进一步求出氯酸钾的质量分数。
考点:利用质量守恒定律定律解有关化学方程式的计算题

 金钥匙试卷系列答案
金钥匙试卷系列答案长时间使用的热水壶底部有一层水垢,主要成分是CaCO3。某校化学研究性学习小组同学通过实验想测定水垢中CaCO3的含量。他们取100g水垢,加入足量的稀盐酸,同时测量5分钟(min)内生成CO2质量,测量数据如下表:
| 时间/ min | 1 | 2 | 3 | 4 | 5 |
| 生成CO2的质量/g | 15 | 25 | 30 | 33 | 33 |
②请根据表格分析写出你发现的一条规律是 。
③该水垢中CaCO3的质量分数是多少?
用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4Cl),该反应可表示为:NaCl+NH4HCO3═NaHCO3+NH4Cl.
20℃时,按上述化学方程式中反应物的质量比,向100g水中加入11.7g NaCl
和15.8g NH4HCO3.请计算:
(1)理论上从溶液中析出晶体的质量为多少g?
(2)反应后所得溶液中溶质NH4Cl的质量分数是多少?(写出计算式即可).
资料:20℃时四种物质的溶解度如下,假设它们同时溶解在水中各自的溶解度不变.
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶解度/g | 36.0 | 21.6 | 37.2 | 9.6 |
铜镁合金具有优良的导电性,常用作飞机天线等导电材料.欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(1)合金中铜、镁的质量比.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)
 2CuSO4+2H2O.若用一定量溶质的质量分数为9.8%的稀硫酸恰好处理2000g含铜3.2%的废料(假设其他杂质不和硫酸反应且不溶于水),求反应后所得硫酸铜溶液中溶质的质量分数.
2CuSO4+2H2O.若用一定量溶质的质量分数为9.8%的稀硫酸恰好处理2000g含铜3.2%的废料(假设其他杂质不和硫酸反应且不溶于水),求反应后所得硫酸铜溶液中溶质的质量分数.
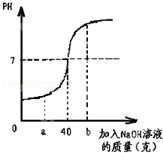
 O2↑+2H2O.请计算:
O2↑+2H2O.请计算: