题目内容
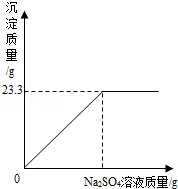
某化学兴趣小组为了测定某稀硫酸的溶质质量分数,取100g稀硫酸于烧杯中,向烧杯中逐滴滴入质量分数为10%的氢氧化钠溶液,反应过程中所得溶液的酸碱度变化如图:
(1)当加入氢氧化钠溶液的质量为a g时,所得溶液中的溶质是 (填化学式);
当加入氢氧化钠溶液的质量为b g时,向所得溶液中滴加酚酞溶液,溶液呈 色。
(2)稀硫酸的溶质质量分数是多少?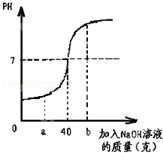
(1)H2SO4、Na2SO4;红; (2)4.9%
解析试题分析:(1)根据图示中关于反应进行时pH的变化情况分析可知:当加入氢氧化钠溶液的质量为a g时溶液的pH小于7,溶液显酸性说明此时硫酸有剩余,所以溶质中含有剩余的硫酸和氢氧化钠与稀硫酸反应生成的硫酸钠;当加入氢氧化钠溶液的质量为b g时,溶液的pH大于7,该溶液呈碱性,所以该溶液能使酚酞试液变红。
(2)依据加入氢氧化钠40g时溶液的pH等于7,说明此时氢氧化钠和稀硫酸恰好反应,据此依据化学方程式的计算求解即可。由图象可知当加入氢氧化钠溶液40g时反应恰好进行;
设稀硫酸的溶质质量分数为x
H2SO4+2NaOH=2H2O+Na2SO4
98 80
100x 40g×10%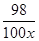 =
=
解得x=4.9%
考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算

 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案现有Cu与另一种金属(可能是Mg、Fe、Zn中的一种)形成的粉末。现欲测定其组成,进行如下实验:取该粉末16g放入烧杯,将溶质质量分数为14%的稀硫酸280.0g分4次加入该烧杯中,充分反应后,测得剩余的固体质量数据记录如下:
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70.0 | 70.0 | 70.0 | 70.0 |
| 剩余固体质量/g | 13.6 | 11.2 | 8.8 | 8.4 |
计算(要求写出计算过程):
(1)该粉末中Cu的质量分数。
(2)该粉末中另一种金属为何种金属。
(3)第3次加入稀硫酸充分反应后,所得溶液中溶质的质量分数。
某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合.加热该混合物t1时间后(杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
(1)加热t3时间后氯酸钾是否已经完全反应? (填是或否).
(2)求完全反应后产生氧气的质量 .
(3)求该样品中氯酸钾的质量分数.