题目内容
为测定实验室中某过氧化氢溶液的溶质质量分数,小明取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验,反应的化学方程式是2H2O2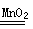 O2↑+2H2O.请计算:
O2↑+2H2O.请计算: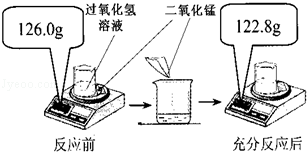
(1)反应后产生氧气的质量为 g。
(2)此过氧化氢溶液的溶质质量分数。
(1)3.2g; (2)27.2%
解析试题分析:(1)根据质量守恒定律,烧杯内质量的减少的质量即生成的氧气的质量。
(2)根据过氧化氢分解的化学方程式和生成氧气的质量,计算出参与反应的过氧化氢的质量,然后根据质量分数公式计算即可。
解:(1)根据质量守恒定律,反应生成氧气的质量=126.0g-122.8g=3.2g;
(2)设这过氧化氢溶液中溶质过氧化氢的质量为x
2H2O2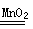 O2↑+2H2O
O2↑+2H2O
68 32
x 3.2g =
=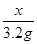
x=6.8g
过氧化氢溶液中溶质质量分数为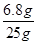 ×100%=27.2%
×100%=27.2%
答:(1)3.2g;(2)过氧化氢溶液中溶质质量分数为27.2%
考点:考查根据化学反应方程式的计算;有关溶质质量分数的简单计算

练习册系列答案
相关题目
某同学为了测定实验室中氯酸钾样品的纯度,取2.5g该样品与0.5g二氧化锰混合.加热该混合物t1时间后(杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热t2、t3、t4时间后剩余固体的质量,记录数据如下表:
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 2.12 | 2.08 | 2.04 | 2.04 |
(1)加热t3时间后氯酸钾是否已经完全反应? (填是或否).
(2)求完全反应后产生氧气的质量 .
(3)求该样品中氯酸钾的质量分数.