题目内容
【题目】下列图像能正确反映对应变化关系的是( )
A.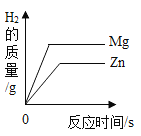 向足量的锌、镁中分别加入等质量、等浓度的稀盐酸
向足量的锌、镁中分别加入等质量、等浓度的稀盐酸
B.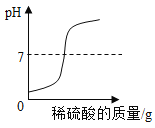 向一定量的氢氧化钠溶液中滳加稀硫酸
向一定量的氢氧化钠溶液中滳加稀硫酸
C.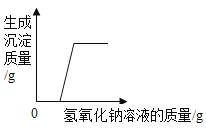 向一定量混有少量盐酸的氯化镁溶液中加入足量氢氧化钠溶液
向一定量混有少量盐酸的氯化镁溶液中加入足量氢氧化钠溶液
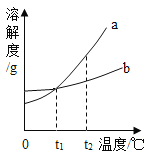
D.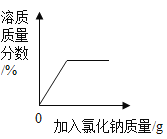 向一定溶质质量分数的不饱和氯化钠溶液中加入氯化钠固体
向一定溶质质量分数的不饱和氯化钠溶液中加入氯化钠固体
【答案】C
【解析】
A、镁的金属活动性比锌活泼,相同时间内产生的氢气,镁大于锌;该反应中稀盐酸的质量一定且少量,镁、锌与盐酸反应产生的气体相同;故图像所示错误。
B、氢氧化钠溶液呈碱性,pH值应大于7,向一定量的氢氧化钠溶液中滴加稀硫酸,pH值应逐渐下降,故图像所示错误。
C、盐酸先和氢氧化钠反应,生成水和氯化钠,没有沉淀产生;盐酸完全反应后,氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠;故图像所示正确。
D、一定溶质质量分数的不饱和氯化钠溶液的质量分数应大于0,起点错误,加入氯化钠固体后,溶质质量增大至饱和,饱和后溶质质量分数不变,故图像所示错误。
故选:C。

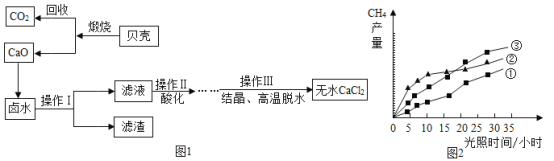
【题目】目前大部分城市居民所使用的燃料主要是管道煤气或天然气,管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4,它们的燃烧反应如下:
2CO+O2![]() 2CO2;2H2+O2
2CO2;2H2+O2![]() 2H2O ;CH4+2O2
2H2O ;CH4+2O2![]() CO2+2H2O
CO2+2H2O
(1)根据以上化学方程式判断,相同条件下,燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是__________,因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是______进风口(填“增大”或“减小”),如不改进可能产生的不良后果是___________。
(2)家庭煤气管常用硬质聚氯乙烯和聚乙烯塑料管,塑料管属于_______材料。
(3)管道煤气中含有的烃类,除甲烷外还有少量乙烷、丙烷、丁烷等的某些性质见下表:
乙烷 | 丙烷 | 丁烷 | |
熔点/℃ | -183.3 | -189.7 | -183.4 |
沸点/℃ | -88.6 | -42.1 | -0.5 |
试根据以上某个关键数据解释冬天严寒季节有时管道煤气火焰很小,并且呈断续状态的原因是:________________。
【题目】请回答下列问题:
(1)铝热反应是焊接铁路上钢轨的反应原理:即在高温下铝与氧化铁发生反应生成氧化铝和铁,写出该反应的化学方程式_____该反应属于_____反应(填基本类型)
(2)下面是部分金属的部分物理性质:
物理性质 | 物理性质比较 |
导电性 |
|
密度 |
|
由上表可知:用铝作高空电缆是因为_____、_____。
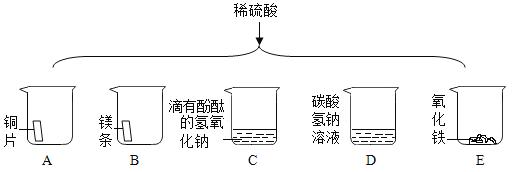
(3)认真观察分析比较下列几个反应及现象:
A “真金不怕火炼”金在高温下也不与氧气发生反应。Au+O2![]() (不反应)
(不反应)
B 金属镁在空气中燃烧,发出耀眼的强光,放出大量的热量。2Mg+O2![]() 2MgO
2MgO
C 铜在加热条件下与氧气发生反应,在表面变黑。2Cu+O2![]() 2CuO
2CuO
D 铝在空气中与氧气发生反应,在表面生成一层致密的氧化膜。2Al+3O2=2Al2O3
从上述实验事实可以看出,四种金属的活动性顺序是_____。