��Ŀ����
����Ŀ���������غ����У���ˮ���̲��ŷḻ����Դ��������ˮ��Դǰ��������̽��ѧϰС���Ժ���Ca2+��Mg2+��Cl�����ӵ�±ˮ�ͱ��ǣ���Ҫ�ɷ�ΪCaCO3��Ϊ��Ҫԭ����ʵ�����Ʊ���ˮCaCl2��������ͼ1��
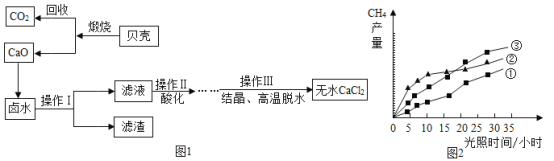
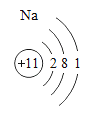
��1������������ƣ�__��
��2���������ữʱӦѡ�������__����д��ѧʽ����
��3����MgCl2Ϊ��д��±ˮ�г�ȥMg2+ʱ������Ӧ�Ļ�ѧ����ʽ__��
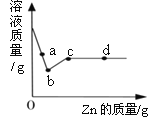
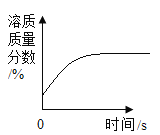
��4�����յ�CO2������������ʹ�������������ˮ������Ӧ������CH4��O2���÷�Ӧ�Ļ�ѧ����ʽΪ__������������ʱ���ڲ�ͬ�������١��ڡ��ۣ��������£�CH4���������ʱ��ı仯��ͼ2��ʾ���ڵ�10СʱʱCH4������ߵ���__����д��������������������������
���𰸡����� HCl MgCl2+Ca��OH��2=CaCl2+Mg��OH��2�� CO2+2H2O CH4+2O2 ��
CH4+2O2 ��
��������
��1��������õ����ǹ����Һ�壬�ǹ��˲�����
��2���ù������Ʊ������Ȼ��ƣ���ѡ�����ֻ�������ᣬ��ѧʽΪ��HCl��
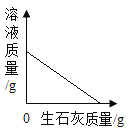
��3���Ȼ�þת��Ϊ������þ�ķ�Ӧ���Ȼ�þ���������Ʒ�Ӧ������������þ�������Ȼ��ƣ���Ӧ�Ļ�ѧ����ʽ�ǣ�MgCl2+Ca��OH��2=CaCl2+Mg��OH��2����
��4��������̼��ˮ�ڴ����������ߵ������������ɼ������������Ӧ�Ļ�ѧ����ʽΪCO2+2H2O CH4+2O2������ͼʾ���Կ������ڵ�10СʱʱCH4������ߵ��Ǣڡ�
CH4+2O2������ͼʾ���Կ������ڵ�10СʱʱCH4������ߵ��Ǣڡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
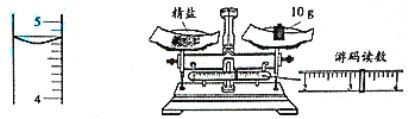
Сѧ��10����Ӧ����ϵ�д�����Ŀ��ijʳƷ��װ���ϵ�˵�����£�
��Ʒ���� | XX���� |
���� | С��ɰ�ǡ�����ֲ���͡��ʼ��������͡�ʳ�Ρ����ɼ���ʳ���㾫 |
��� | 400g |
���ط��� | �����������ˬ������������ֱ�� |
������ | 270�� |
�������� | XXXX��XX��XX�� |
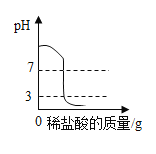
��1�������ֱ��ɵ������У����������ʵ���______________��������֬����_____________�������ǣ�C6H12O6����������֯����ø�Ĵ������·�����Ӧ�Ļ�ѧ����ʽΪ________________��
��2����֪�������к�N����������ԼΪ15%������һ�������˴�ʳ������ȡ�ĵ����ʾ��������³´�л����ȫת��Ϊ����CO(NH2)2�ų����⣬ÿ���ų�����25g�����������ÿ���ʳ������ȡ�ĵ����ʵ�����������________g���г���ʽ���ɣ���
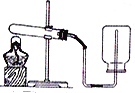
����Ŀ����ͼ��ijȼ����ˮ�����ڲ�����ʾ��ͼ��
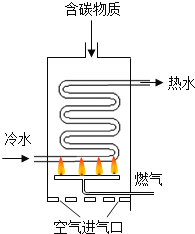
��1����ˮ������Ȼ��Ϊȼ������Ȼ������________������������������������Դ��ȼ����ˮ���е��Ƚ����������˻��ιܽṹ�����ŵ���___________��
��2����ֵ��ָ1kgij��ȼ����ȫȼ�շų�����������������ȼ�ϵ���ֵ��1kgȼ��ȼ�ղ�����CO2��SO2���������±�������±�������������ȼ����������Ч����Դ����Ȼ����������____________��
ȼ�� | ȼ�����������/g | |
������̼ | �������� | |
���� | 2900 | 5.0 |
��Ȼ�� | 2500 | 0.1 |
ú | 2500 | 11.0 |
��3��Ŀǰ���������ø����ȸ������۵�ũ�����Ʊ��ƾ�����������ø��������ת��Ϊ�����ǣ������ǣ���ѧʽ��C6H12O6���ھƻ�ø�����������ɾƾ����������ЧӦ�����壬��д��������ת��Ϊ�ƾ��Ļ�ѧ����ʽ��_____________��