题目内容
【题目】某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。
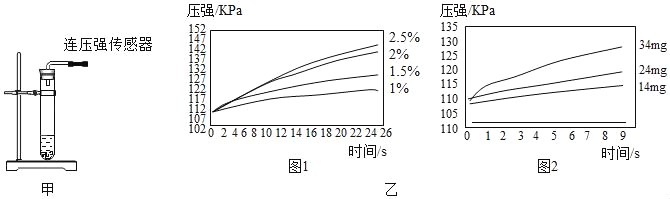
(解释与结论)
(1)过氧化氢溶液制取氧气的化学方程式为_______________。
(2)实验1得到的结论是___________________________。实验2的目的是_________。
欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比____________。(简要的写出实验设想)
(3)小组同学通过互联网得知:多种物质能催化过氧化氢的分解。
(实验探究)
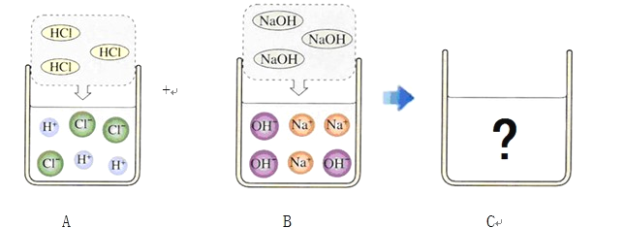
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42﹣ ),稀硫酸中含有三种粒子(H2O、H+、SO42﹣ )为了进一步探究CuSO4,溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H2O,他们的理由是____________。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
实验步骤 | 实验现象 | 结论 |
a 取一支试管加入5mL 5%过氧化氢溶液,然后加入2﹣3滴稀硫酸 | 溶液几乎没有 气泡放出 | 验证明,起催化作用的是______。 |
b.另取一支试管加入5mL 5%过氧化氢溶液,然后加入2﹣3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是__________、_________。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?_____。理由是________。
【答案】2H2O2![]() 2H2O+O2↑。其他条件相同的情况下,过氧化氢的浓度越大,反应越快;其他条件相同的情况下,二氧化锰质量对过氧化氢分解速率的影响;过氧化氢质量分数相同,加和不加二氧化锰的两种情况下压强变化的情况。过氧化氢溶液中含有水;Cu2+;过氧化氢的浓度低;催化剂的量太少。:不合理;水受热转化为水蒸气导致气压变化。
2H2O+O2↑。其他条件相同的情况下,过氧化氢的浓度越大,反应越快;其他条件相同的情况下,二氧化锰质量对过氧化氢分解速率的影响;过氧化氢质量分数相同,加和不加二氧化锰的两种情况下压强变化的情况。过氧化氢溶液中含有水;Cu2+;过氧化氢的浓度低;催化剂的量太少。:不合理;水受热转化为水蒸气导致气压变化。
【解析】
(1)过氧化氢溶液与MnO2制取氧气,是过氧化氢在二氧化锰的催化下生成水和氧气,反应方程式为2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(2)根据实验1对应的图标可以看出,在相同的时间内,质量分数越大的过氧化氢容易导致装置内的压强越大,也就是生成的氧气越多,即反应越快,所以实验1得到的结论是其他条件相同的情况下,过氧化氢的浓度越大,反应越快。根据实验2对应的图标可以看出,在相同的时间内,加入的二氧化锰的质量越大的过氧化氢容易导致装置内的压强越大,也就是生成的氧气越多,即反应越快,实验2的目的是其他条件相同的情况下,二氧化锰越多反应越快;欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比过氧化氢质量分数相同,而加和不加二氧化锰的两种情况下压强变化的情况。
(3)①催化剂在化学反应前后质量和化学性质不变;某同学认为最不可能的是H2O,他的理由是过氧化氢溶液中含有水;②溶液中稀硫酸以氢离子和硫酸根离子的形式存在,当加入稀硫酸后,溶液几乎没有气泡冒出,说明氢离子和硫酸根离子对过氧化氢没有催化作用;硫酸铜溶液中溶质以硫酸根离子和铜离子的形式存在,当加入 过氧化氢溶液中后,溶液中有大量的气泡冒出,说明起到了催化作用,由ab对比实验可知,其催化作用的是铜离子。
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少,这可能是过氧化氢的浓度低或催化剂的量太少造成的。
(5)过氧化氢分解放热,水受热转化为水蒸气造成气压改变,所以不能利用图甲装置探究“温度对过氧化氢分解速率”的影响;

 阅读快车系列答案
阅读快车系列答案【题目】“从生活走进化学,从化学走向社会”。请你用化学知识回答以下问题:
(1)社会实践小组的同学到敬老院给李奶奶送去鲜花和生日蛋糕。花香满屋,请用微粒的观点解释闻到香味的原因________________;蛋糕沾到手上,用洗手液洗干净,这是利用了洗涤剂的__________作用。
(2)河水中含有许多杂质,可利用吸附沉淀过滤和蒸馏等方法净化,其中净化程度最高的方法是_____;杀菌消毒时,会用到消毒泡腾片,其有效成分为二氧化氯(ClO2),氯元素的化合价为_____________。
(3)家庭厨房就是一个化学小世界,“锅碗瓢盆”和“柴米油盐”中包含着许多化学知识:
①下列厨房用具的主要材料,属于有机合成材料的是_____(填序号)

②均衡膳食有利于人体健康。小强家某天午饭的食谱如下表:
主食 | 馒头 |
副食 | 红烧排骨、花生米、清蒸鱼 |
饮料 | 牛奶 |
从营养学的角度考虑,你建议在食谱中应该增加_____(填序号)
A.油饼B.烧豆腐C.凉拌黄瓜D.炒鸡蛋
(4)汽车是重要的交通工具。请回答以下问题:
①汽车使用天然气作为燃料,排放污染较低。天然气的主要成分为___________。
②完成汽车用铅酸电池充电的反应:2PbSO4+2______= Pb+2H2SO4+PbO2(填化学式)。