题目内容
【题目】下图是教材中验证质量守恒的定律的实验,请回答相关问题:
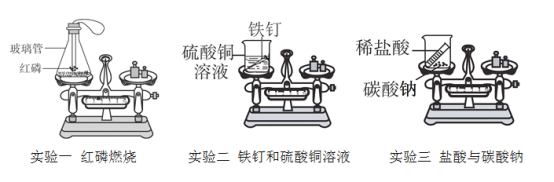
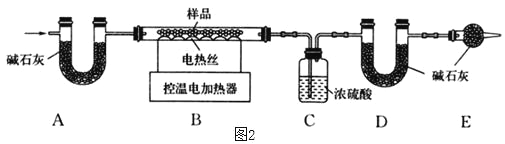
(1)实验一,先将胶塞上的玻璃管末端加热至红热,再接触瓶内红磷,其目的是________;
(2)实验二,铁与硫酸铜(CuSO4)溶液作用生成硫酸亚铁(FeSO4)和铜,写出该反应的化学方程式 ________;
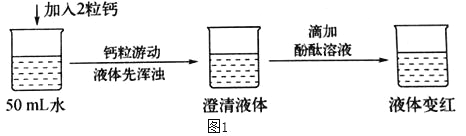
(3)实验三,碳酸钠与稀盐酸反应的化学方程式为Na2CO3+2HCl═2NaCl+CO2↑+X,其中X的化学式为________,这个反应后烧杯中物质的质量减少的原因是________;
(4)为了验证质量守恒定律,在选择化学反应和装置时应注意的问题是________。
【答案】点燃红磷Fe+CuSO4=FeSO4+CuH2O由于装置未密封,导致生成的二氧化碳逸散到空气中如用有气体参加或生成的反应来验证质量守恒定律时,装置应密封
【解析】
(1)实验一中先将胶塞上的玻璃管末端加热至红热,再接触瓶内红磷,是为了在锥形瓶内引燃红磷。(2)铁的金属活动性比铜的强,能将铜从其盐溶液中置换出来,二者反应的化学方程式为Fe+CuSO4===FeSO4+Cu。(3)根据质量守恒定律可知,化学反应前后各元素原子的总数不变。反应前各元素原子数为Na:2,C:1,O:3,H:2,Cl:2,反应后为Na:2,C:1,O:2,H:0,Cl:2,比反应前少2个氢原子,1个氧原子,故X的化学式为H2O。因为该反应装置未密封,导致生成的二氧化碳气体逸出到空气中,未能称量,所以反应后烧杯中物质的质量减少。(4)根据实验三可知,在使用有气体参加或生成的反应来验证质量守恒定律时,装置应密封,防止气体逸出,导致称量的结果不准确。

【题目】某小组同学在用过氧化氢溶液与MnO2制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。为此,他们进行了如下探究:
(猜想与假设)
①速度慢、气泡少可能与过氧化氢溶液的浓度有关。
②速度慢、气泡少可能与MnO2的质量有关。
(进行实验)
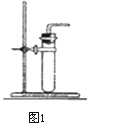
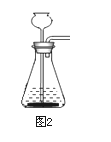
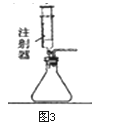
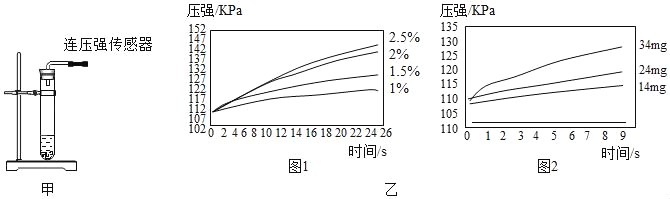
根据图甲进行如下实验。
实验1:用26mg MnO2与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量MnO2进行实验,压强变化如乙图2。
(解释与结论)
(1)过氧化氢溶液制取氧气的化学方程式为_______________。
(2)实验1得到的结论是___________________________。实验2的目的是_________。
欲得出“MnO2对过氧化氢分解有催化作用”的结论,需要对比____________。(简要的写出实验设想)
(3)小组同学通过互联网得知:多种物质能催化过氧化氢的分解。
(实验探究)
实验证明,CuSO4溶液也能显著加快过氧化氢的分解,CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42﹣ ),稀硫酸中含有三种粒子(H2O、H+、SO42﹣ )为了进一步探究CuSO4,溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计。
①小组同学认为最不可能的是H2O,他们的理由是____________。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
实验步骤 | 实验现象 | 结论 |
a 取一支试管加入5mL 5%过氧化氢溶液,然后加入2﹣3滴稀硫酸 | 溶液几乎没有 气泡放出 | 验证明,起催化作用的是______。 |
b.另取一支试管加入5mL 5%过氧化氢溶液,然后加入2﹣3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
(反思与评价)
(4)小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是__________、_________。
(5)利用图甲装置探究“温度对过氧化氢分解速率”的影响,是否合理?_____。理由是________。