题目内容
【题目】用恰当的化学用语和数字填空
(1)两个氧原子_____;
(2)氯化亚铁中的阳离子_____;
(3) 2个碳酸根离子_____;
(4)氧化铁中铁元素的化合价_____;
(5)硫酸钠中硫酸根显-2价_____;
(6)硫酸铝_____;
(7)氦气_____;
(8)3个铵根离子_____;
(9)碳酸钠中碳元素的化合价_____;
(10)保持水的化学性质的最小粒子_____;
【答案】2O Fe2+ 2CO32- ![]()
![]() Al2(SO4)3 He 3NH4+
Al2(SO4)3 He 3NH4+ ![]() H2O
H2O
【解析】
(1)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以2个氧原子,就可表示为:2O;
(2)氯化亚铁中的阳离子是亚铁离子,可以表示为Fe2+;
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个碳酸根离子可表示为:2CO32-;
(4)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此氧化铁中铁元素的化合价表示为:![]() ;
;
(5)硫酸钠中硫酸根显-2价就是在硫酸钠化学式中硫酸根符号的正上方加上-2,故填:![]() ;
;
(6)硫酸铝中铝元素为+3价,硫酸根为-2价,硫酸铝的化学式为Al2(SO4)3,故填:Al2(SO4)3;
(7)氦是稀有气体元素,由稀有气体元素组成的单质是单原子分子,所以氦气的化学式就是表示氦元素的元素符号,即:He;
(8)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故3个铵根离子可表示为:3NH4+;
(9)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以碳酸钠中碳元素的化合价,故可表示为:![]() ;
;
(10)保持水的化学性质的最小粒子是水分子,其化学式为:H2O。

【题目】厨房里有很多的化学物质,某同学对厨房的调味品进行了调查研究。
Ⅰ食盐是重要的调味品。缺碘会引起甲状腺肿大,如图是厨房中某“加碘盐”的标签,下列说法正确的是___________。

A碘盐中的“碘”指的是碘原子
B碘盐中含有钠原子、氯原子等微粒
C碘酸钾易溶水
D碘酸钾的化学性质很稳定
Ⅱ蔗糖也是常用的调味品。对蔗糖的制备及成分进行如下探究。
一、蔗糖的工业制备:工业制备蔗糖的流程如图所示。
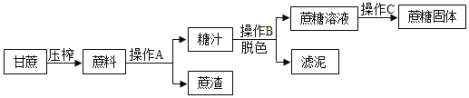
(1)糖汁呈棕黄色,工业上可加入___________(填一种化学物质)对糖汁进行脱色处理。
(2)由甘蔗制得蔗糖的整个过程中主要是___________(选填“物理”或“化学”)变化。
二、蔗糖组成探究
(资料卡片)
①绿色植物吸收空气中的CO2和H2O先合成葡萄糖,再将葡萄糖转化为蔗糖。
②蔗糖不易燃烧,掺入少量烟灰后,就能直接点燃(烟灰不能燃烧)。烟灰可能的作用为___________。
(成份探究)
实验操作 | 实验现象 | 实验结论 | |
实验1 | 点燃蔗糖与烟灰混合物,在火焰上方罩一干冷烧杯 | 烧杯壁有水雾 | 说明蔗糖中含有___________元素。 |
实验2 | 取下烧杯迅速加入澄清石灰水,振荡 | ___________ | 说明蔗糖中含有碳元素 |
实验3 | 取少量蔗糖隔绝空气高温加热 | 容器内壁出现水雾,生成黑色固体 | 说明蔗糖中还含有___________元素。 |
(计算验证)
已知:化学变化中,分子的种类发生改变,而原子的种类、个数和质量都不发生改变。现称取34.2g蔗糖,加入少量烟灰点燃,测得生成52.8g CO2和19.8g H2O。则34.2g蔗糖中,碳元素的质量为___________g,氢元素的质量为___________g。通过综合计算,可知蔗糖的化学式为___________(选填字母)。
AC6H5NO2 BC6H12O6 CC12H22 DC12H22O11
【题目】过氧化氢俗称双氧水,常温下是一种无色液体,性质比较稳定。在加热的条件下,它能分解生成氧气和水。查阅资料:
①将新制的浓度5%的双氧水加热到65℃时就有氧气产生,加热到80℃时就有较多氧气产生。
②若在相同质量5%的双氧水中加入少量二氧化锰固体,常温下就会立即产生氧气,反应速度快,所需时间短。
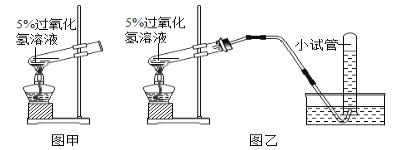
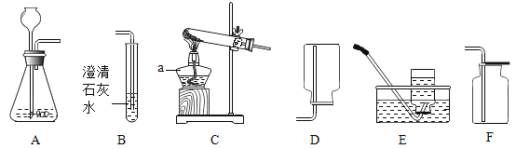
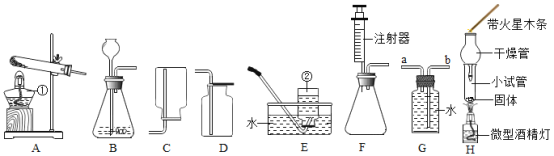
请根据上图回答问题:
(1)请你写出用双氧水和二氧化锰混合物制取氧气的反应文字表达式:____________
(2)小红按图甲装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,他利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星木条未复燃的原因是__________________。
(3)以下是某小组同学探究影响过氧化氢分解速率部分因素的相关实验数据。
实验序号 | H2O2溶液 浓度% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
① | 5 | 5 | 20 | 0.1 | 4 | 16.75 |
② | 15 | V | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 0 | 2 | 49.21 |
④ | 30 | 5 | 55 | 0 | 2 | 10.76 |
①V=________:从实验_________和__________(填序号)对比可知,过氧化氢分解速率与过氧化氢溶液浓度有关。从表中实验数据对比可知,过氧化氢分解速率与温度的关系是:___
②用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量__(填“减小”“不变”或“增大”)。
(注意:若正确回答下列问题加4分,总分不超过60分)
③除了上述影响因素外,过氧化氢分解生成氧气的速率还与哪些因素有关?请你继续探究。(写出一种假设,并设计实验方案)
(你的假设)___________
(设计方案)
实验方法及步骤 | 可能观察到的实验现象 | 实验结论 |
_________ | _________ | 假设正确 |