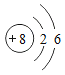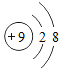题目内容
【题目】宏观、微观之间存在必然的联系,建立正确的微粒观有助于化学的学习。请用微粒的知识回答下列问题。
(1)原子内部含有带电荷的质子和电子,而整个原子不显电性的原因是_______________。
(2)“醋酸糖甜”是因为_____________。
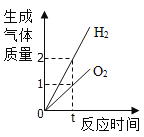
(3)(相关信息:物质在发生化学反应前后元素的种类和质量都不变)气体X在氧气中燃烧生成5.6g氮气和10.8g水,X分子中一定含有的原子是______________(填符号),气体X中一定所含元素的质量比是_______________。
【答案】原子中,质子数等于电子数,电量相等,电性相反 不同分子,性质不同 N和H 氮元素(N):氢元素(H)=14:3
【解析】
(1)原子中,质子数等于电子数,电性相反,电量相等,正负抵消,所以整个原子不显电性;
(2)“醋酸糖甜”是因为分子构成不同,性质不同。
(3)气体X在氧气中燃烧生成氮气和水,由质量守恒定律可知反应前后原子的种类不变,X分子中一定含有的原子是N和H。N和H的质量比是![]() 。
。

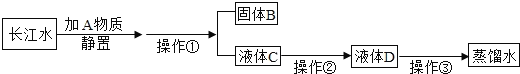
【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究:

(集体讨论):
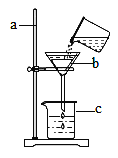
(1)小组同学共同设计了如图的两套装置,你认为合理的是_____(填字母)。
(2)为了确保实验成功,在装药品前应先_____。
(分组实验)在讨论的基础上,他们分组进行了实验.
(数据分析)实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入瓶中体积水的体积 | 20 | 21 | 19 | 20 | 22 | 18 |
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_____。
(实验拓展)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体,如红磷。
(4)小红提出可以用细铁丝代替红磷,小雯不赞成,她的理由是_____。
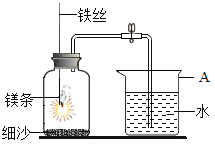
(5)小刚选择镁条探究空气中氧气的含量,装置见下图,用砂纸打磨镁条的目的是_____。燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积_____%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成推测减少的气体中有氮气。
(发现问题)氮气是怎样减少的呢?
(假设一)氮气与镁条反应而减少。
(假设二)氮气与_____反应而减少。
(查阅资料)镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。该反应的符号表达式_____。
(反思总结)①测定空气中氧气含量不能选择镁带。
②物质燃烧_____(选填“一定”或“不一定”)需要氧气。
(计算拓展)①氮化镁中氮元素化合价为_____。
②试计算6g氮化镁中含多少质量的镁元素?_____
【题目】下表中与各粒子名称对应的各项内容均正确的是( )
选项 | 内容粒子名称 | 符号 | 结构示意图 | 电性 | 化学性质 |
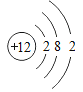
A | 镁原子 | Mg |
| 中性 | 活泼易得电子 |
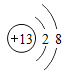
B | 铝原子 | Al3+ |
| 带3个单位正电荷 | 活泼 |
C | 氧原子 | O |
| 中性 | 稳定 |
D | 氟离子 | F- |
| 带一个单位负电荷 | 稳定 |
A. AB. BC. CD. D
【题目】空气是一种宝贵的资源。请回答下列问题:
(1)清洁的空气对于人类非常重要,下列做法有利于保护大气的是_______ (填序号,下同)。
a使用清洁能源 b燃放烟花爆竹 c大量植树 d推广私家汽车出行
(2)空气中下列气体过多会引起温室效应的是_______
a二氧化氮 b一氧化碳 c二氧化碳 d二氧化硫
(3)空气污染指数与质量状况的对应关系:
污染指数 | 0-50 | 51-100 | 101-200 | 201-300 | 301以上 |
质量状况 | 优 | 良 | 普通 | 不佳 | 差 |
某市区某天的空气污染指数为48,首要污染物为:可吸入颗粒物。根据以上信息,判断该市区当天的空气质量状况是(____________)
A优 B良 C轻度污染 D重度污染
(4)某化学兴趣小组用红磷测定空气中氧气含量,分6组测定(注:集气瓶容积为100mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/ml | 20 | 21 | 15 | 20 | 22 | 19 |
根据上述测定,计算空气中氧气体积分数为_________________