题目内容
【题目】归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应)。
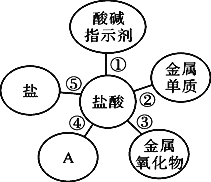
(1)为了验证性质①,小红将紫色石蕊溶液加到盐酸中,溶液变__________色。
(2)盐酸的性质③决定了盐酸可用于清除铁锈,写出该反应的化学方程式:____________,该反应的实验现象是________。
(3)为验证性质⑤,应选用的物质是________(写一种物质的名称)。
【答案】红 Fe2O3+6HCl═2FeCl3+3H2O 铁锈溶解,溶液由无色变成黄色 硝酸银
【解析】
(1)石蕊遇酸性溶液会变红色,所以将紫色石蕊试液滴加到盐酸溶液中溶液变红;故填:红。
(2)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;该反应的现象是铁锈溶解,溶液由无色变成黄色;故填:Fe2O3+6HCl═2FeCl3+3H2O;铁锈溶解,溶液由无色变成黄色;
(3)酸与盐的反应一定要符合复分解反应的发生条件,所以选择的盐与盐酸反应时一定会有水、气体或沉淀生成.所以该盐可以是硝酸银;故填:硝酸银。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究:

(集体讨论):
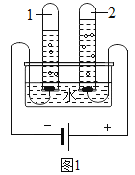
(1)小组同学共同设计了如图的两套装置,你认为合理的是_____(填字母)。
(2)为了确保实验成功,在装药品前应先_____。
(分组实验)在讨论的基础上,他们分组进行了实验.
(数据分析)实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入瓶中体积水的体积 | 20 | 21 | 19 | 20 | 22 | 18 |
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_____。
(实验拓展)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体,如红磷。
(4)小红提出可以用细铁丝代替红磷,小雯不赞成,她的理由是_____。
(5)小刚选择镁条探究空气中氧气的含量,装置见下图,用砂纸打磨镁条的目的是_____。燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积_____%。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成推测减少的气体中有氮气。
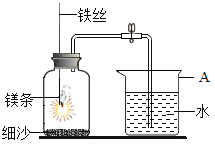
(发现问题)氮气是怎样减少的呢?
(假设一)氮气与镁条反应而减少。
(假设二)氮气与_____反应而减少。
(查阅资料)镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。该反应的符号表达式_____。
(反思总结)①测定空气中氧气含量不能选择镁带。
②物质燃烧_____(选填“一定”或“不一定”)需要氧气。
(计算拓展)①氮化镁中氮元素化合价为_____。
②试计算6g氮化镁中含多少质量的镁元素?_____
【题目】在测定空气中氧气含量的实验中,赵敏采用了如图所示装置:由两个注射器组成的密闭容器中留有25mL空气(不考虑玻璃管内气体的体积),给装有细铜丝的玻璃管加热,同时交替缓慢推动两个注射器的活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却后,将气体推至一个注射器内,观察密闭装置内空气体积的变化。
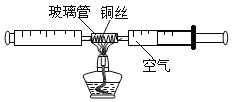
(资料)铜丝在加热时与空气中的氧气反应生成黑色的氧化铜固体。
(1)在加热过程中,交替缓慢推动两个注射器的活塞的目的是_____。
(2)写出该实验中反应的文字表达式:_____。
(3)赵敏测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 21mL |
由此数据可以推算出她测定的空气中氧气的体积分数_____21%(填“>”“<”或“=”)。造成该实验出现误差的原因可能是_____(填序号,多选)
①装置气密性差
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
【题目】空气是一种宝贵的资源。请回答下列问题:
(1)清洁的空气对于人类非常重要,下列做法有利于保护大气的是_______ (填序号,下同)。
a使用清洁能源 b燃放烟花爆竹 c大量植树 d推广私家汽车出行
(2)空气中下列气体过多会引起温室效应的是_______
a二氧化氮 b一氧化碳 c二氧化碳 d二氧化硫
(3)空气污染指数与质量状况的对应关系:
污染指数 | 0-50 | 51-100 | 101-200 | 201-300 | 301以上 |
质量状况 | 优 | 良 | 普通 | 不佳 | 差 |
某市区某天的空气污染指数为48,首要污染物为:可吸入颗粒物。根据以上信息,判断该市区当天的空气质量状况是(____________)
A优 B良 C轻度污染 D重度污染
(4)某化学兴趣小组用红磷测定空气中氧气含量,分6组测定(注:集气瓶容积为100mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/ml | 20 | 21 | 15 | 20 | 22 | 19 |
根据上述测定,计算空气中氧气体积分数为_________________