题目内容
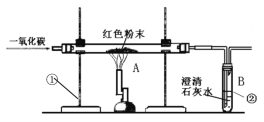
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)①氧化铜(CuO)为黑色固体。②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,
(进行实验)
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 | 1—1 | 1—2 |
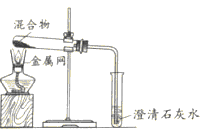
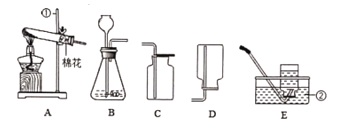
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
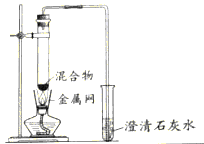
实验2:取一定量的混合物,用1—2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2—1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2—2 | 1:10 | 混有很少量黑色物质 | |
2—3 | 1:11 | 混有极少量黑色物质 | |
2—4 | 1:12 | 无黑色物质 | |
2—5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)配平化学方程式:□C+□CuO高温 □Cu+ □CO2↑______,这个反应中CuO是______剂。
(2)实验1—2中,证明此产生了CO2的现象是__________,写出化学方程式______________
(3)实验1的目的是___________。
(4)实验2的结论是:木炭与氧化铜反应的最佳质量比为_______。
【答案】1221 氧化 澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓ +H2O 比较受热面积对C与CuO反应的影响 1:12
【解析】
(1)木炭与氧化铜反应方程式:C+2CuO高温2Cu+CO2↑,该反应中氧化铜失氧成为铜单质,发生的是还原反应,所以是氧化剂;
(2)二氧化碳使澄清石灰水变浑浊,发生的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,反应方程式为:CO2 + Ca(OH)2 == CaCO3↓+ H2O;
(3)实验1-1,反应物接触面积较大,实验1-2反应物接触面积较小,可以探究木炭与氧化铜的受热面积对其反应的影响;
(4)碳和氧化铜都是黑色固体,铜为紫红色固体,反应后有黑色固体剩余,说明有剩余的碳或氧化铜,由表格信息可知,当木炭与氧化铜质量比为1:12时无黑色物质剩余,说明恰好反应,即木炭与氧化铜反应的最佳质量比为1:12。

 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案【题目】某化学研究小组对当地的石灰石样品进行研究。称取石灰石样品8g,把50g稀盐酸分五次加入样品中,测得实验数据见下表(假设石灰石样品中的杂质不溶于水、不与盐酸反应,二氧化碳不溶解,氯化钙易溶于水)。
实验序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第1次 | 10 | 6 |
第2次 | 10 | 4 |
第3次 | 10 | 2 |
第4次 | 10 | 1 |
第5次 | 10 | m |
请回答:(1)第5次剩余固体的质量m=__________g;
(2)石灰石样品中CaCO3的质量分数为多少_________?(写出计算过程,下同)
(3)反应结束后生成CO2的质量是多少_________?