题目内容
【题目】实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验。
配制溶质质量分数为10%氢氧化钠溶液100g。
(1)所需的氢氧化钠质量______g;需要水的质量__________,体积为________mL(水的密度为1g/cm3)。
(2)称量时,氢氧化钠固体应放于天平_____(填“左”或“右”)盘的烧杯内;量取所需要的水,应选择的量筒的规格是_______mL(选填“10”、“100”或“250”)。
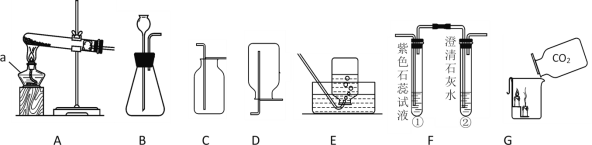
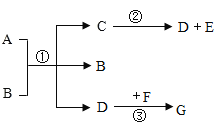
(3)配制的操作如下图,正确操作顺序为________(填字母);
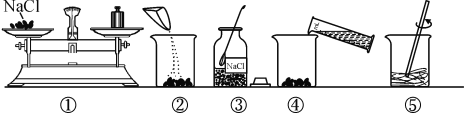
A.③①②④⑤ B.①③④②⑤ C.③①④②⑤ D.①④③②⑤
(4)下列错误操作可能导致溶液溶质质量分数偏大的是______ (填序号)。
①操作中砝码和食盐放置颠倒 ②食盐中混有少量不溶性杂质 ③量取水时俯视量筒读数 ④装瓶时有部分溶液洒落到瓶外 ⑤溶解食盐的烧杯内壁有水
【答案】10 90g 90 左 100 A ③
【解析】
(1)配制溶质质量分数为10%氢氧化钠溶液100g,所需的氢氧化钠质量为100g×10%=10g,故填10;
需要水的质量=溶液质量-溶质质量=100g-10g=90g,故填90g;
需要谁的体积为90g÷1g/cm3=90 mL故填90。
(2)用天平称取物质时,被称物应放到天平的左盘,故填左;
用量筒量取90mL水,应选择规格为100mL的量筒,故填100。
(3)配置一定溶质质量分数的溶液操作过程是:取药品放到天平上,称取一定质量的药品,将称好的药品加到烧杯中,再将量好的溶剂倒入放有固体溶质的烧杯中,溶解,所以正确的操作顺序是③①②④⑤,故选A。
(4)①操作中砝码和食盐放置颠倒,称得药品质量往往少于要求量,配的溶液溶质质量分数小于要求值,选项错误; ②食盐中混有少量不溶性杂质,称得食盐质量小于要求量,配的溶液溶质质量分数小于要求值,选项错误; ③量取水时俯视量筒读数,读数大于实际值,取得溶剂的实际量小于要求量,配的溶液溶质质量分数大于要求值,选项正确; ④装瓶时有部分溶液洒落到瓶外,不影响溶质质量分数,选项错误;⑤溶解食盐的烧杯内壁有水,增大了溶剂的质量,配的溶液溶质质量分数小于要求值,选项错误,故选③。

【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)①氧化铜(CuO)为黑色固体。②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,
(进行实验)
实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 | 1—1 | 1—2 |
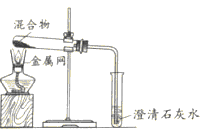
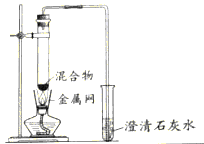
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定量的混合物,用1—2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2—1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2—2 | 1:10 | 混有很少量黑色物质 | |
2—3 | 1:11 | 混有极少量黑色物质 | |
2—4 | 1:12 | 无黑色物质 | |
2—5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)配平化学方程式:□C+□CuO高温 □Cu+ □CO2↑______,这个反应中CuO是______剂。
(2)实验1—2中,证明此产生了CO2的现象是__________,写出化学方程式______________
(3)实验1的目的是___________。
(4)实验2的结论是:木炭与氧化铜反应的最佳质量比为_______。