题目内容
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____。
(查阅资料)CaCl2溶液显中性。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2;猜想Ⅱ:有CaCl2和HCl;猜想Ⅲ:有CaCl2和Ca(OH)2;猜想Ⅳ:有CaCl2、HCl和Ca(OH)2。
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_______。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
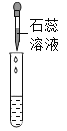
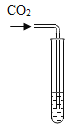
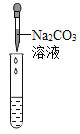
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ①______ | ②_______ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因:_____。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑____。
【答案】2HCl+Ca(OH)2=CaCl2+2H2O HCl和Ca(OH)2不能共存 石蕊溶液变蓝 溶液变浑浊 CaCl2与Na2CO3反应也会生成白色沉淀,不能证明一定有Ca(OH)2存在 反应物是否过量
【解析】
[演示实验]将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中,稀盐酸和氢氧化钙反应生成氯化钙和水,该反应的化学方程式是:Ca(OH)2+2HCl═CaCl2+2H2O;
[猜想与假设]乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是稀盐酸和氢氧化钙不能共存;
[实验探究]氢氧化钙溶液显碱性,能使石蕊试液变蓝色,能和二氧化碳反应生成碳酸钙沉淀和水,能和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;故填:石蕊溶液变蓝;溶液变浑浊。
[评价反思](1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,原因是碳酸钠和氯化钙反应也能生成白色沉淀碳酸钙;
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑反应物是否过量。

 名师导航单元期末冲刺100分系列答案
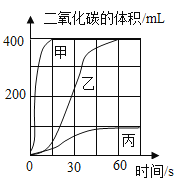
名师导航单元期末冲刺100分系列答案【题目】实验室制备并收集二氧化碳,按下表进行实验。取等质量的同种大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图所示。下列说法错误的是
实验编号 | 药品 |
Ⅰ | 块状大理石、10% H2 SO4溶液 |
Ⅱ | 块状大理石、7% HCl溶液 |
Ⅲ | 大理石粉末、7% HCl溶液 |
A.实验Ⅲ对应的左图变化曲线为甲
B.实验II和Ⅲ对比,说明影响反应速率的因素是固体的颗粒大小
C.实验I和Ⅱ对比,说明影响反应速率的因素是酸的浓度
D.实验Ⅱ和Ⅲ完全反应后,产生二氧化碳的质量是相等的
【题目】(1)请根据下列实验装置回答问题
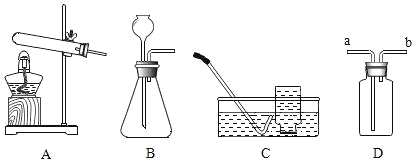
①实验室制取氧气的发生装置可选用_____(选填一个字母),对应反应的化学方程式是_____。如果用排水法收集氧气,当_____时开始收集。
②制取气体时,在连接好仪器、加入药品前必须进行的操作是_____;气体从b管通入C装置时,可以收集的一种气体是_____。
(2)老师:酚酞指示剂是酚酞溶解在60﹣90%的酒精溶液中形成的
A同学:溶质是_____。
老师:Good!
A同学:酚酞溶液为什么只有淡淡的酒精气味?
B同学:是因为_____。
老师:你从微观解释,好极了!
C同学:老师,如果用水配制酚酞指示剂可以吗?
老师:有想法,很好!你们可以进行实验探究。
实验后,学生实验报告如下,请你补充完整。
(实验目的)_____。
(查阅资料)
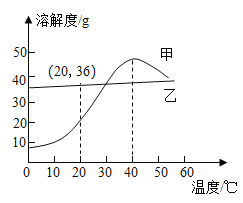
①20℃时,在水中,酚酞的溶解度是0.2g;在酒精中,酚酞的溶解度是20g。
②配制酚酞指示剂的传统方法:1g酚酞溶于1L60﹣90%的酒精溶液中
(实验用品)
实验药品:酚酞、_____、澄清石灰水
实验仪器:试管、烧杯、玻璃棒、_____、托盘天平、量筒(合适的规格)、容器(2L、3L、4L、5L)
(实验方案)
20℃时,称取0.2g酚酞溶于120mL水中配成溶液,将此溶液平分到4个容器中并加水稀释成2L、3L、4L、5L,分别将稀释后的酚酞溶液滴入到澄清石灰水中,观察颜色变化并记录于如表:
酚酞溶液的种类 | 滴入滴数 | 澄清石灰水/mL | 现象 |
2L | 2﹣3 | 2﹣3 | 深红 |
3L | 2﹣3 | 2﹣3 | 深红 |
4L | 2﹣3 | 2﹣3 | 红 |
5L | 2﹣3 | 2﹣3 | 浅红 |
(反思与评价)
①极稀的酚酞水溶液遇碱有明显的颜色变化,_____(填“可以”或“不可以”)作指示剂。
②配制酚酞指示剂_____(填“有”或“没有”)必要用酒精溶液。
③对此实验探究,你的认识是_____。