题目内容
【题目】按下列要求完成化学方程式
(1)木炭在氧气中燃烧______。
(2)过氧化氢溶液与二氧化锰混合______。
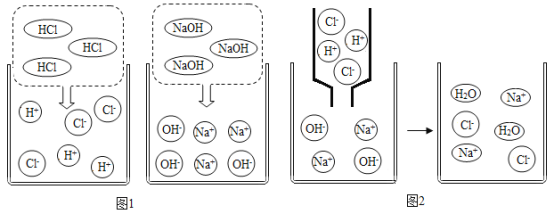
(3)氢氧化钠和硫酸溶液反应______。
【答案】C+O2![]() CO2 2H2O2
CO2 2H2O2![]() 2H2O+O2↑ 2NaOH+H2SO4=Na2SO4+2H2O
2H2O+O2↑ 2NaOH+H2SO4=Na2SO4+2H2O
【解析】
首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可。
(1)在点燃的条件下,碳与氧气反应生成二氧化碳;故填:C+O2![]() CO2;
CO2;
(2)在二氧化锰的催化作用下,过氧化氢分解为水和氧气;故填:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)氢氧化钠和硫酸反应生成硫酸钠和水;故填:2NaOH+H2SO4=Na2SO4+2H2O。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】“84”消毒液在日常生活中使用广泛,具有漂白、杀菌、消毒功效。某化学兴趣小组对一瓶敞口久置的“84”消毒液成分产生兴趣,在老师的指导下进行如下探究:
(提出问题)该敞口久置的“84”消毒液中溶质有哪些?
(查阅资料)“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO为有效成分,有腐蚀性并易与空气中CO2反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。次氯酸(HClO)溶液和次氯酸钠(NaClO)溶液都具有漂泊、杀菌、消毒功效。HClO不稳定,受热或光照易分解。
(分析讨论)小组同学经过讨论,认为:一定含有____,可能还有NaClO、HClO、Na2CO3中的一种或几种。
(设计方案)为验证猜想,设计如下方案:
实验操作 | 实验现象 | 结论 |
Ⅰ、向盛有有色布条的烧杯中滴加该消毒液适量,放置一段时间 | 布条不褪色 | 该消毒液中___ |
Ⅱ、另取该消毒液少量于试管中,滴加足量氯化钙溶液,震荡 | _ | 该消毒液中含有Na2CO3 |
实验Ⅱ中的反应化学方程式为____;
(得出结论)综上所述,该敞口久置的“84”消毒液中溶质有__。
(交流反思)生活中,“84”消毒液贮藏时应注意_。一般不要“84”消毒液对蔬菜、水果进行消毒,其原因可能是_。
(拓展延伸)(1)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为____
(2)次氯酸钠与盐酸反应可生成有毒的氯气,日常生活中“84”消毒液不能与洁厕灵(主要成分为盐酸)混合使用。
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____。
(查阅资料)CaCl2溶液显中性。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2;猜想Ⅱ:有CaCl2和HCl;猜想Ⅲ:有CaCl2和Ca(OH)2;猜想Ⅳ:有CaCl2、HCl和Ca(OH)2。
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_______。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
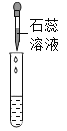
实验操作 |
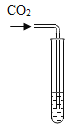
|
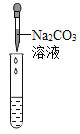
|
|
实验现象 | ①______ | ②_______ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因:_____。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑____。