题目内容
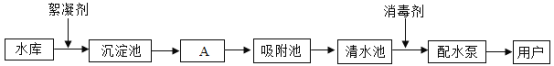
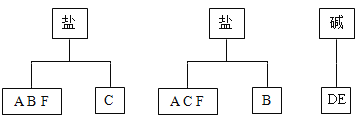
【题目】A、B、C、D、E、F是初中化学实验室常用的6种白色固体物质,由氢、碳、氧、氯、钠和钙元素组成。实验教师按其类别放置在药品柜中,下图是以上各种药品摆放的示意图(矩形表示药品柜)。其中,4种盐有两种摆放方式。
(1)B是唯一难溶于水的物质,其化学式为__________。
(2)E的溶液可与A的溶液反应生成D的溶液,其化学方程式为_________________。
(3)证明A、B、F含有部分相同的组成,所需试剂是_____________________________。
(4)C可由其他三种物质分别转化而成,图中的反应①是中和反应,该反应的化学方程式为______________________________。请将这三种物质的代号按照反应的编号填入下图中①是_______、②是_______、③是_______。

【答案】CaCO3 ![]() 稀盐酸和澄清石灰水
稀盐酸和澄清石灰水 ![]() D A F(A、F可以换位置)
D A F(A、F可以换位置)
【解析】
(1)B为唯一难溶于水的物质,从题目给出的元素中,只有碳酸钙为难溶于水的物质,所以B为碳酸钙,化学式为CaCO3;
故答案为:CaCO3。
(2)D和E都是碱,碱是由金属离子和氢氧根离子组成,而上述元素中只有钠和钙两种元素,所以D和E是在氢氧化钠和氢氧化钙中选择,B为碳酸钙,属于碳酸盐,而A与B属于同一种盐类,所以A也是碳酸盐,A中碳酸根与钙离子可以生成碳酸钙,所以E是含有钙离子的氢氧化钙,而D就为氢氧化钠,根据质量质量守恒定律,则A就是碳酸钠,所以A碳酸钠与E氢氧化钙反应生成碳酸钙和D氢氧化钠,所以该反应的化学方程式为![]() ;
;
故答案为:![]() 。
。
(3)根据(1)和(2)可知A为碳酸钠,B为碳酸钙,D为氢氧化钠,E为氢氧化钙,ABF和C是两类盐,A和B为碳酸盐,所以F属于碳酸盐类,所以F可以是碳酸氢钠,三种盐都可与盐酸反应生成二氧化碳,气体通入澄清石灰水后,澄清石灰水变浑浊,从而证明其含有部分相同的组成,所以可以借助稀盐酸和澄清石灰水检验;
故答案为:稀盐酸和澄清石灰水。
(4)C可以由其他三种物质制得,而在ADF中都含有钠,且都可以与盐酸反应生成氯化钠,所以C为氯化钠,而生成C氯化钠的反应①属于中和反应,则推出①处是氢氧化钠与盐酸反应生成氯化钠和水,②和③处是碳酸钠、碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,所以②和③处可以任填A和F;
故答案为:![]() ;D;A;F。(A、F可以换位置)
;D;A;F。(A、F可以换位置)

【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
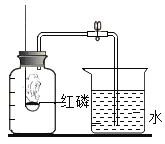
(演示实验)将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____。
(查阅资料)CaCl2溶液显中性。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想Ⅰ:只有CaCl2;猜想Ⅱ:有CaCl2和HCl;猜想Ⅲ:有CaCl2和Ca(OH)2;猜想Ⅳ:有CaCl2、HCl和Ca(OH)2。
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_______。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
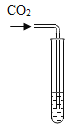
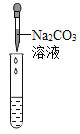
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | ①______ | ②_______ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因:_____。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑____。