��Ŀ����
����Ŀ��Ϊ̽��̼��ԭ����ͭ�����ʵ����������ľ̿�ۺ�����ͭ�ĸ�������1��2.5g����ϵ��ʵ�顣
���������ϣ�̼��ԭ����ͭ�õ���ͭ�п��ܺ���������ɫ��������ͭ������ͭԪ�صĻ��ϼ�Ϊ+1�ۣ���
������ʵ�飩ʵ��1��ȡ������Ϊ1��11��ľ̿�ۺ�����ͭ�����1.3g������ʵ�顣
��� | 1��1 | 1��2 |
װ�� |
|
|
��Ӧ�����ʵ���ɫ��״̬ | ��ɫ��ĩ�л���������ɫ���� | ��ɫ�����н��������м�������ɫ���� |
ʵ��2��ȡһ�����Ļ�����1��2װ�ý���ʵ�顣
��� | ľ̿��������ͭ�������� | ��Ӧ�����ʵ���ɫ��״̬ | |
2��1 | 1��9 | ��ɫ�����н������� | ����������ɫ���� |
2��2 | 1��10 | ���к�������ɫ���� | |
2��3 | 1��11 | ���м�������ɫ���� | |
2��4 | 1��12 | ��ɫ���� | |
2��5 | 1��13 | ���н϶��ɫ���� | |
��1��������ͭ�Ļ�ѧʽΪ_____��
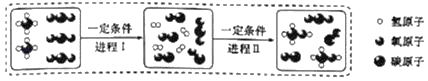
��2��ʵ��1��2�У�֤�������˶�����̼��������_____����صĻ�ѧ��Ӧ����ʽΪ_____��
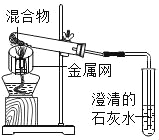
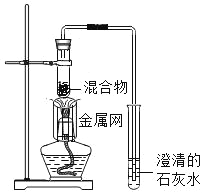
��3��ʵ��1��2�У�����Ӧ�������Ƚ������ܴ�ʯ��ˮ��ȡ����Ȼ��ر�ֹˮ�У��ò�����Ȼ��ȴ�������ر�ֹˮ�У����ܳ��ֵ�������_____��
��4��ʵ��1��Ŀ����_____��
��5��ʵ��2�Ľ�����_____��
����˼�����ۣ�
��1����ͬѧ�����ó�ϸ̿��������ͭ��ĩ����ʵ�顣����Ϊ���������������_____��
��2��ʵ��2δ����������Ϊ1��14��ʵ�飬������_____��
���𰸡�Cu2O ����ʯ��ˮ����� CO2+Ca��OH��2��CaCO3��+H2O ����������Թ��У�ʹ���ɵ����ȵ�ͭ���±����� ̽������ͭ��ľ̿������������䷴Ӧ��Ӱ�� ľ̿������ͭ������Ϊ1��12ʱǡ����ȫ��Ӧ�����ľ̿������ͭ��Ӧ�����������Ϊ1��12 �����˷�Ӧ��֮��ĽӴ��������Ӧ���еø���� ľ̿������ͭ��������Ϊ1��13ʱ������ͭ�ѹ�������
��������
[����ʵ��]��1��������ͭ�У�ͭԪ����+1�ۣ���Ԫ����-2�ۣ�����������ͭ�Ļ�ѧʽΪCu2O��
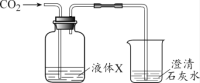
��2��������̼���������Ʒ�Ӧ����̼��ư�ɫ������ˮ����ѧ��Ӧ����ʽΪ��CO2+Ca��OH��2=CaCO3��+H2O�����Զ�����̼��ʹ�����ʯ��ˮ����ǣ���֤��������CO2�������dz���ʯ��ˮ����ǣ�
��3������Ӧ�������Ƚ������ܴ�ʯ��ˮ��ȡ����Ȼ��ر�ֹˮ�У��ò�����Ȼ��ȴ�������ر�ֹˮ�У����ܳ��ֵ������ǿ���������Թ��У�ʹ���ɵ����ȵ�ͭ���±�������
��4��ʵ��1��ʵ��1-1�����������������ʵ��1-2�л������������������̽������ͭ��ľ̿������������䷴Ӧ��Ӱ�죻
��5��ʵ��2�ṩ�������Լ�ʵ��������Կ�����ľ̿������ͭ������Ϊ1��12ʱǡ����ȫ��Ӧ�����ľ̿������ͭ��Ӧ�����������Ϊ1��12��
[��˼������]��1����ϸ̿��������ͭ��ĩ�ĽӴ������Ӧ����֣�
��2��ľ̿������ͭ��������Ϊ1��13ʱ������ͭ�ѹ���������û�б�Ҫ����������Ϊ1��14��ʵ�顣