��Ŀ����
����Ŀ����Һ�����ǵ�����������ء�
��1���������������ʷֱ����ˮ�У���ֽ�����ܵõ���ɫ��Һ����_____������ĸ����
A���������
B������
C������
D�����
��2����ʢ��ˮ���ձ��м�������ij�����ʣ��γ���Һ�����У��¶��������ߵ���_____������ĸ����
A���ռ�
B�������
C���Ȼ���
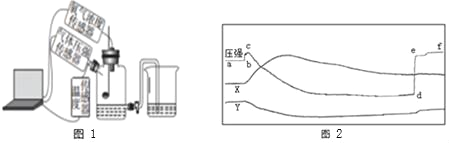
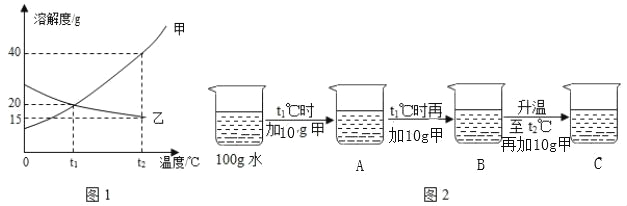
��3����ͼ1Ϊ�ס������ֹ������ʵ��ܽ�����ߡ�
���ܽ�����¶����߶���С��������_____����ס����ҡ�����
�ڰ�ͼ2��ʾ����ʵ�飬�õ���Ӧ�¶��µ�A��B��C��Һ����A��B��C������Һ�����ڱ�����Һ����_____������ĸ��������ҺC���ټ���25g�ף���ֽ��裬�ָ���t2��ʱ��������Һ�����ʵ���������Ϊ_____�������ȷ��0.1%����
�۽�t2��ʱ�ļס����������ʵı�����Һ������t1�棬������Һ�����ʵ�������������_____�ң��������������������
���𰸡�C A �� B 28.6% ��
��������
��1�������������ˮ�õ���ɫ��Һ�����͡����������ˮ����������ˮ�γ���ɫ��Һ��
��2��������������ˮ����Һ�¶��������ߣ����������ˮ����Һ�¶Ȼ������䣻�Ȼ�������ˮ����Һ�¶Ȼ������䣻
��3����ͨ�������ܽ�����߿�֪���ܽ�����¶����߶���С���������ң�
��t1��ʱ�������ʵ��ܽ����20g��t2��ʱ�������ʵ��ܽ����40g����ͼ2��ʾ����ʵ�飬�õ���Ӧ�¶��µ�A��B��C��Һ���ܼ�����10g�����ʷֱ���10g��20g��30g��������A��B��C������Һ�����ڱ�����Һ����B������ҺC���ټ���25g�ף���ֽ��裬�����������55g���ָ���t2��ʱ��������Һ�����ʵ���������Ϊ![]() ��100%=28.6%��
��100%=28.6%��
�۽�t2��ʱ�ļס����������ʵı�����Һ������t1�棬�����ʵ��ܽ�ȼ�С�������ʵ��ܽ������Ӧ�ð���t2��ʱ���ܽ�ȼ��㣬����������Һ�����ʵ������������ף��ҡ�

 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
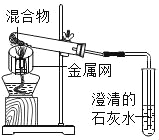
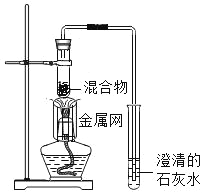
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�����Ŀ��̼��ԭ����ͭ��ʵ������ͼ��ʾ��д���÷�Ӧ�Ļ�ѧ����ʽ____��
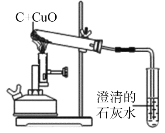
��������⣩̼ȼ��ʱ��������CO2Ҳ��������CO����ô̼������ͭ��Ӧ���ɵ������Ƿ�Ҳ�ж��ֿ��ܣ�
���������룩����٣�CO
����ڣ�CO2
��ۣ�____________��
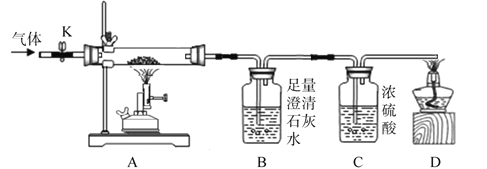
����Ʒ�����ʵ��װ����ͼ��Ũ���������ˮ���ã�����K������ͨ�����ĵ���һ��ʱ�䣬�ر�K����ȼ�ƾ���ƺ;ƾ��ƣ���ַ�Ӧ��Ϩ��ƾ���ƺ;ƾ��ƣ���K����ͨһ��ʱ�䵪����
����һ���Ӷ��Թ۲�Ƕ��ж�
��1��ʵ��ʱA����������____________��
��2��������ٳ�����B��D����������_____________������ţ���
a��B�б���ǣ�D���ܵ�ȼ������������������b��B�б���ǣ�D�����ܵ�ȼ
c��B��������ʵ������D���ܵ�ȼ������ d��B��������ʵ������D�����ܵ�ȼ
���������Ӷ�������Ƕ��ж�
ȡһ����̿�ۺ�4g����ͭ�Ļ�������ʵ�飬���ⶨ�����е��ĸ����ݣ�
��Ӧǰ������ | ��Ӧ������� | |
A��������+���壩 | m1 | m2 |
B+C�����ƿ+���Һ�� | m3 | m4 |
��3��������ڳ������������ϣ�m4-m3��__��m1-m2����ѡ���������������=������
��4��������۳�����CuOȫ��ת����Cu����μӷ�Ӧ��̼������m��ȡֵ��Χ��____��
��������˼��ʵ�鿪ʼǰ����ͨ�뵪����Ŀ����____��
����Ŀ��Ϊ̽��̼��ԭ����ͭ�����ʵ����������ľ̿�ۺ�����ͭ�ĸ�������1��2.5g����ϵ��ʵ�顣
���������ϣ�̼��ԭ����ͭ�õ���ͭ�п��ܺ���������ɫ��������ͭ������ͭԪ�صĻ��ϼ�Ϊ+1�ۣ���
������ʵ�飩ʵ��1��ȡ������Ϊ1��11��ľ̿�ۺ�����ͭ�����1.3g������ʵ�顣
��� | 1��1 | 1��2 |
װ�� |
|
|
��Ӧ�����ʵ���ɫ��״̬ | ��ɫ��ĩ�л���������ɫ���� | ��ɫ�����н��������м�������ɫ���� |
ʵ��2��ȡһ�����Ļ�����1��2װ�ý���ʵ�顣
��� | ľ̿��������ͭ�������� | ��Ӧ�����ʵ���ɫ��״̬ | |
2��1 | 1��9 | ��ɫ�����н������� | ����������ɫ���� |
2��2 | 1��10 | ���к�������ɫ���� | |
2��3 | 1��11 | ���м�������ɫ���� | |
2��4 | 1��12 | ��ɫ���� | |
2��5 | 1��13 | ���н϶��ɫ���� | |
��1��������ͭ�Ļ�ѧʽΪ_____��
��2��ʵ��1��2�У�֤�������˶�����̼��������_____����صĻ�ѧ��Ӧ����ʽΪ_____��
��3��ʵ��1��2�У�����Ӧ�������Ƚ������ܴ�ʯ��ˮ��ȡ����Ȼ��ر�ֹˮ�У��ò�����Ȼ��ȴ�������ر�ֹˮ�У����ܳ��ֵ�������_____��
��4��ʵ��1��Ŀ����_____��
��5��ʵ��2�Ľ�����_____��
����˼�����ۣ�
��1����ͬѧ�����ó�ϸ̿��������ͭ��ĩ����ʵ�顣����Ϊ���������������_____��
��2��ʵ��2δ����������Ϊ1��14��ʵ�飬������_____��