题目内容
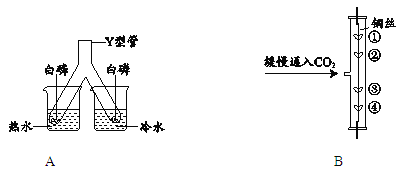
【题目】某校化学学习小组用如图所示装置电解水,为加快电解速率,该小组同学采用了澄清石灰水代替蒸馏水进行电解实验。请回答下列问题:
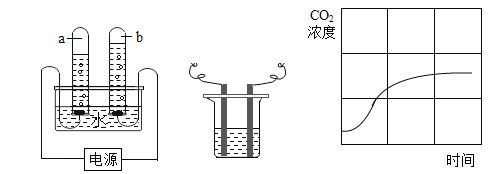
(1)试管a中的气体为 ___________(填化学式),试管b连接的是电源的__________极。电解水的化学方程式为________。
(2)实验时该组同学采用石墨棒作为电极,在电解过程中发现澄清石灰水变浑浊了。针对此异常现象,该小组进行了如下探究。
(提出猜想)
(1)电解过程中水不断减少,导致溶液中的氢氧化钙不能继续溶解,形成沉淀。
(2)电解过程中,温度升高,导致溶液中的氢氧化钙不能溶解,形成沉淀。
(进行实验)
(1)另取相同浓度、相同体积的澄清石灰水,加入 10mL 蒸馏水,搅拌,在相同电压下再次进行电解实验,电解相同时间,观察到溶液仍然是浑浊的,这说明:_____。
(2)取 100mL 相同浓度的澄清石灰水于大烧杯中,加热至电解实验时上升的温度,没有观察到浑浊。这说明:______。
(3)该小组采用铂电极电解澄清石灰水,发现澄清石灰水没有变浑浊,于是提出猜想该澄清石灰水变浑浊的原因可能与____有关。
(4)另取浑浊的液体,向其中加入稀盐酸,并用二氧化碳传感器测量反应产生的二氧化碳浓度。据此推测该浑浊中应该有:____。产生该物质的原因可能是:_______,______(请用化学方程式表示)。
(5)实验最终表明该猜想正确,但实验过程中该小组同学也发现,向浑浊的液体中滴加盐酸,并没有气泡产生。其原因可能是_______。
【答案】H2 正 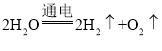 溶液变浑浊不是水减少,导致溶液中的氢氧化钙不能继续溶解而析出 溶液变浑浊不是由于温度升高导致的 用石墨棒作为电极 碳酸钙
溶液变浑浊不是水减少,导致溶液中的氢氧化钙不能继续溶解而析出 溶液变浑浊不是由于温度升高导致的 用石墨棒作为电极 碳酸钙 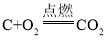
![]() 滴加的稀盐酸量较少,稀盐酸和氢氧化钙反应生成氯化钙和水,反应不产生气泡
滴加的稀盐酸量较少,稀盐酸和氢氧化钙反应生成氯化钙和水,反应不产生气泡
【解析】
水在通电的条件下负极生成氢气,正极生成氧气,碳和氧气在点燃的条件下生成二氧化碳、二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,稀盐酸与氢氧化钙反应生成氯化钙和水,稀盐酸与碳酸钙反应生成氯化钙、水和二氧化碳。
(1)水在通电的条件下负极生成氢气,正极生成氧气,氧气和氢气的体积比是1:2,故试管a中的气体为H2,试管b生成氧气,故连接的是电源的正极,电解水的化学方程式为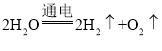 。
。
[进行实验]
(1)在相同电压下再次进行电解实验,观察到溶液仍然是浑浊的,说明溶液变浑浊不是水减少,导致溶液中的氢氧化钙不能继续溶解而析出。
(2)氢氧化钙的溶解度随温度的升高而减小,所以取100mL相同浓度的澄清石灰水于大烧杯中,加热至电解实验时上升的温度,没有观察到浑浊,说明溶液变浑浊不是由于温度升高导致的,故这说明溶液变浑浊不是由于温度升高导致的。
(3)采用铂电极电解澄清石灰水,发现澄清石灰水没有变浑浊,于是提出猜想该澄清石灰水变浑浊的原因可能与用石墨棒作为电极有关。
(4)另取浑浊的液体,向其中加入稀盐酸,并用二氧化碳传感器测量反应产生的二氧化碳浓度,所得数据如图,则该浑浊中有碳酸钙,碳和氧气在点燃的条件下生成二氧化碳、二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,故产生该物质的原因可能是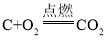 、
、![]() 。
。
(5)加入稀盐酸后,稀盐酸先与氢氧化钙反应生成氯化钙和水,反应不产生气泡,氢氧化钙完全反应后,稀盐酸与碳酸钙反应生成氯化钙、水和二氧化碳,故向浑浊的液体中滴加盐酸,并没有气泡产生,原因可能是滴加的稀盐酸量较少,稀盐酸和氢氧化钙反应生成氯化钙和水,反应不产生气泡。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将150g氯化钙溶液分四次加入,充分反应,四次测量所得数据如下表所示:
次数 | 累计加入氯化钙溶液的质量/g | 烧杯中溶液的总质量/g |
一 | 40 | 134 |
二 | 80 | 168 |
三 | 120 | 202 |
四 | 150 | 232 |
(1)恰好完全反应时,生成沉淀的总质量为____g。
(2)第四次测量时,所得溶液中的溶质有_______(填化学式)。
(3)计算氯化钙溶液的溶质质量分数为______________(写出计算过程)。
【题目】化学在人类社会的发展历程中起着重要作用。正确认识物质

(1)请在上表中方框内填写对应的元素符号____。
(2)Mg、Sn、Pt、Au四种金属,能与稀盐酸或稀硫酸发生置换反应的有_____种。
(3)合理利用资源化学小组通过实验将生锈铁钉回收处理。
实验过程 | 实验现象 | 实验原理 | 保存方法 |
a.向装有生锈铁钉的烧杯中加入稀盐酸,浸没铁钉 | 溶液由无色变为黄色、铁钉表面有气泡产生、铁锈脱落 | 请写出稀盐酸除铁锈的化学方程式___ | 写出一条防止铁制品生锈的方法:___ |
b.取出铁钉,洗涤、干燥,妥善保管 | 铁钉呈现银白色 |
小组同学提出,烧杯中的废液也可以回收处理。
同学们查阅相关资料,获知:
a Fe2O3是一种红棕色粉末,俗称铁红,常用作红色油漆和涂料
b FeCl2十2NaOH=Fe(OH)2↓+ 2NaCl
c 4Fe(OH)2+O2+2H2O=4Fe(OH)3
d 不溶性碱受热易分解.生成对应的金属氧化物和水
实验流程:
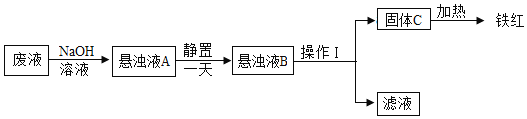
(4)请回答:
①悬浊液A静置一天的原因是_______
②操作I的名称是_____