题目内容
【题目】控制变量法是科学实验中的重要方法。下列两个实验的设计均运用了控制变量的方法。
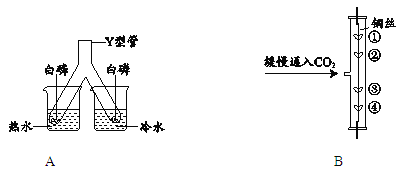
(1)A是探究燃烧条件的实验。实验中观察到浸在 (填“热水”或“冷水”)里的
Y型管中白磷燃烧;该实验中控制的变量是 。
(2)B是探究二氧化碳性质的实验。图中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。能说明CO2密度大于空气且能与水反应的现象为 。
【答案】(1)热水 可燃物、氧气
(2)④比①先变红,②、③不变红
【解析】
试题分析:A是探究燃烧条件的实验。实验中观察到浸在热水里的Y型管中白磷燃烧;该实验中控制的变量是可燃物、氧气;探究二氧化碳性质的实验。图中①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。能说明CO2密度大于空气的是④比①先变红能说明与水反应的现象为②、③不变红,而①④变红。

【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用。
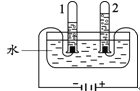
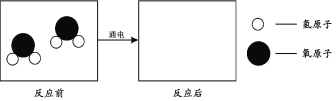
(1)电解水实验揭示了水的组成。右图实验中得到氢气的试管是 (填“1”或“2”);电解水的微观示意图如下,请在方框中补全相应微粒的图示。
(2)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将600 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为 g。
(3)根据下表回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 /g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
①40 ℃时,向两个分别盛有40 g NaCl和NH4Cl的烧杯中,各加入100g的水,充分溶解后,为饱和溶液的是 溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法不正确的是 (填字母序号)。
A.溶质的质量不变 B.溶液质量一定增大
C.可升高温度或增加溶剂 D.溶液中溶质的质量分数一定减小




