题目内容
某化工厂生产的纯碱产品(含有少量氯化钠)的包装袋上注明:碳酸钠≥96%.
为了测定该产品中碳酸钠的质量分数是否属实,向4个分别盛有浓度相同、质量均为100g稀盐酸的烧杯中,分别放入不同质量的纯碱产品,充分反应后,称量烧杯中剩余物的质量,实验数据如下表:
| 所称量的物质 | 实验1 | 实验2 | 实验3 | 实验4 |
| 加入纯碱产品质量/g | 2.8 | 5.6 | 11.2 | 14 |
| 烧杯中剩余物质量/g | 101.7 | 103.4 | 106.8 | 109.6 |
请计算(最后结果保留一位小数):
(1)该纯碱产品中碳酸钠质量分数的标注是否真实.
(2)所用盐酸溶液中溶质的质量分数.
(3)恰好完全反应时,所得溶液中溶质的质量分数.
解析试题分析:盐酸完全反应时,生成二氧化碳的质量为100 g﹢11.2 g﹣106.8 g﹦4.4 g.
设:纯碱产品中碳酸钠质量为x,稀盐酸中溶质的质量为y,生成氯化钠的质量为z.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 117 44
x y z 4.4 g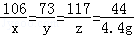
x="10.6" g y="7.3" g z="11.7" g
(1)纯碱产品中碳酸钠的质量分数=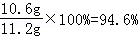 标注不真实.
标注不真实.
(2)盐酸溶液中溶质质量分数=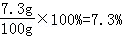
(3)氯化钠溶液中溶质质量分数=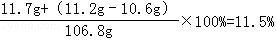
答:(1)该纯碱产品中碳酸钠质量分数的标注不真实.
(2)所用盐酸溶液中溶质的质量分数为7.3%.
(3)恰好完全反应时,所得溶液中溶质的质量分数为11.5%.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.

练习册系列答案
相关题目
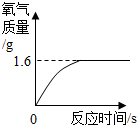
某同学需测定某100g过氧化氢溶液中所含过氧化氢的质量。他取10g二氧化锰放入烧杯中,并将该过氧化氢溶液全部加入,不同时间用电子天平测量其质量,所得读数如下表所示:
| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 烧杯及所盛物质总质量/g | 335.70 | 334.30 | 334.00 | 333.50 | 333.00 | 332.50 | 332.50 |
(1)试分析,100g过氧化氢溶液完全反应后生成氧气的质量为 。(2分)
(2)计算100g过氧化氢溶液中过氧化氢质量分数为多少?(写出计算过程)(6分)
(3)请分析该方法测定结果可能会偏大的原因有 (写出一点即可)(2分)
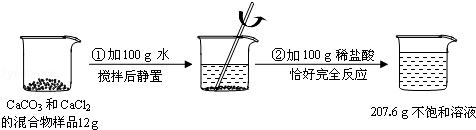
某校化学兴趣小组同学用一瓶含有少量氯化钠的硫酸钠固体样品,进行如下图所示的实验。
已知:Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl
请根据以上信息,计算反应后所得溶液中溶质的质量分数。
为测定黄铜(锌铜合金)样品的组成,某同学取四个样品分别加稀硫酸做了四次实验,其实验数据记录如下表..
| 实验次数 | l | 2 | 3 | 4 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
(1)反应的化学方程式
(2)列出计算黄铜中参加反应的金属质量(X)的比例式:
(3)参加反应的稀硫酸的溶质质量分数
(4)向第一次实验所得溶液中加入47.4g水,溶液中溶质的质量分数
(5)若工业上用125t含Cu2S 70%的辉铜矿炼制该黄铜,理论上能炼制出黄铜的质量为 。