题目内容
科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径。图甲是实验室制取并检验CO2的装置,图乙是对图甲实验装置的“微型”化改进后的装置。 
(1)图乙中微型塑料滴管在实验中的作用与图甲中的 仪器相同(填字母编号)。
(2)通常用甲装置完成该实验需要的盐酸是“微型”实验装置用量的10倍,采用“微型”实验装置具有的优是 。
用乙装置完成“制取并检验CO2”的实验,消耗了含0.1克碳酸钙的石灰石。请计算实验过程中产生CO2的质量是多少克?
(1)A (2)药品用量少,产生的废弃物也少,操作方便 (只答出一点得0.5分,答出两点或两点以上得1分), (3)0.044克
解析试题分析:(1)图乙中微型塑料滴管在实验中的作用与图甲中的分液漏斗相同,故选A;(2)因为通常用甲装置完成该实验需要的盐酸是“微型”实验装置用量的10倍,采用“微型”实验装置具有的优是药品用量少,乙实验装置比甲实验装置操作方便;
(3)设实验过程中产生CO2的质量是x克
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
0.1g x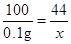
x =0.044g
考点:利用化学方程式计算。

某化工厂生产的纯碱产品(含有少量氯化钠)的包装袋上注明:碳酸钠≥96%.
为了测定该产品中碳酸钠的质量分数是否属实,向4个分别盛有浓度相同、质量均为100g稀盐酸的烧杯中,分别放入不同质量的纯碱产品,充分反应后,称量烧杯中剩余物的质量,实验数据如下表:
| 所称量的物质 | 实验1 | 实验2 | 实验3 | 实验4 |
| 加入纯碱产品质量/g | 2.8 | 5.6 | 11.2 | 14 |
| 烧杯中剩余物质量/g | 101.7 | 103.4 | 106.8 | 109.6 |
请计算(最后结果保留一位小数):
(1)该纯碱产品中碳酸钠质量分数的标注是否真实.
(2)所用盐酸溶液中溶质的质量分数.
(3)恰好完全反应时,所得溶液中溶质的质量分数.
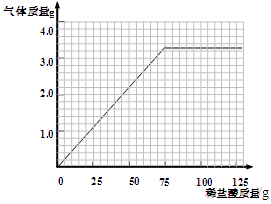
某同学为测定某大理石中碳酸钙(假设:大理石中的杂质不与盐酸反应)的质量分数,取四份样品分别加稀盐酸反应,其实验数据记录如下:
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 取稀盐酸质量(g) | 25.0 | 50.0 | 75.0 | 100.0 |
| 产生气体质量(g) | 1.1 | X | 3.3 | 3.3 |
请计算:
(1)经过分析,在第1次测得的数据中, (填物质)完全反应了;
(2)表格中X= g;
(3)该大理石样品中碳酸钙的质量分数是多少?
(4)画出在10.0g样品中加稀盐酸的质量与产生气体质量变化关系的示意图;