题目内容
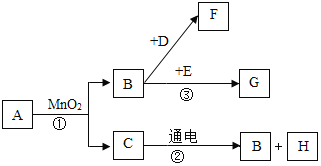
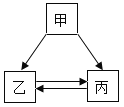
【题目】甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质;乙通常为液体,在一定条件下可分解生成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去)。
(1)甲分解生成乙和丙的化学式反应式为_____。
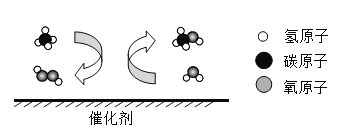
(2)从微观的角度解释甲、乙性质有差异的原因是_____。
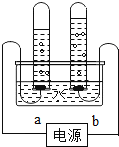
(3)选择合适物质,让丙生成乙,化学反应式为_____。
【答案】2H2O2![]() 2H2O+O2↑ 分子构成不同 2H2+O2
2H2O+O2↑ 分子构成不同 2H2+O2![]() 2H2O
2H2O
【解析】
甲、乙、丙三种物质均含地壳中含量最多的元素,所以均含氧元素,甲、乙是组成元素完全相同的化合物,丙是单质,所以丙是氧气,乙通常为液体,在一定条件下可分解生成丙,甲会分解生成氧气和乙,所以甲是过氧化氢溶液,乙是水,经过验证,推导正确;
(1)甲分解生成乙的反应是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;故填:2H2O2
2H2O+O2↑;故填:2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(2)水和过氧化氢化学性质不同的原因是分子构成不同,故填:分子构成不同。
(3)氧气和氢气在点燃条件下生成水,反应的方程式为2H2+O2![]() 2H2O;故填:2H2+O2
2H2O;故填:2H2+O2![]() 2H2O。
2H2O。

 阅读快车系列答案
阅读快车系列答案【题目】甲乙两化学兴趣小组的同学按课本上的实验装置做“测定空气中氧气的体积分数”实验(如图甲所示),但测出的氧气的体积分数存在误差。

请你参与探究:
甲组测出氧气的体积分数小于五分之一
(提出问题)造成误差的原因是什么?如何改进课本上的实验装置?
(查阅资料)红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(猜想与假设)
A同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性。
B同学:可能是瓶内残留气体中还有氧气。
(1)你还能作出的猜想是____________________________。
(交流与讨论)
他们对课本上的实验装置进行了图乙所示的改进(其他仪器忽略)。
(2)与课本上的实验装置相比较,该装置的一个优点是 _______________。
(3)能得出空气中氧气约占五分之一体积的实验现象是 _______________。
乙组同学从课本镁条燃烧实验得到启发,用镁代替红磷,实验完毕,冷却后进入水的体积远大于总容积的1/5。
(猜想与假设)可能镁条与氮气发生了反应
(设计实验)
为检验镁条能否在N2中燃烧,兴趣小组展开如下探究:

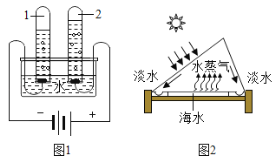
①组装仪器(图1,钟罩下端无底),检查气密性:向水槽中加水,观察现象;
②将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞;
③待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
④打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2),观察液面变化;
(交流讨论)
(4)步骤①气密性良好的现象是________________________;
(5)步骤②目的是_____________________________________;
(6)步骤④观察到_____________________现象,说明镁条与氮气反应。
(结论)除氧气外,镁条还能与氮气反应。
(反思)乙组小罗同学认为只进行图2实验,当钟罩内进入水的体积大于总容积的1/5,就能说明镁与氧气、氮气都发生了反应,对此观点你认为是否正确_______,并说明理由__________________ 。
(拓展)①镁与氮气反应生成氮化镁(Mg3N2),由于氧气比氮气活泼,所以镁燃烧生成的氮化镁质量比氧化镁_______(大、小)。
②8g镁在空气中燃烧,若有30%的镁生成氮化镁,计算氮化镁的质量__________(写出计算过程)。