��Ŀ����
����Ŀ���������仯�����������������й㷺��Ӧ�á�
(һ)����Ʒ�ķ���
��1��������Ҫ�ɷ���Fe2O3�qxH2O����������Ҫ������е�_____________�йء�
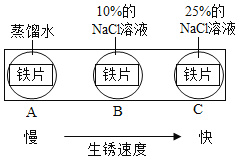
��2����ͼʵ��˵��NaCl���������е�������_______________��
(��)�����Ļ�������
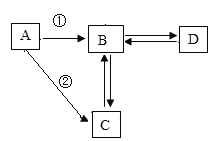
ijƷ�Ƶ����ķϾɵ�·���л���Fe��Cu��Ag��Ni(������ɫ����)�Ƚ�������ͼ��ij������ղ��ֽ����Ĺ������̣���֪��![]()
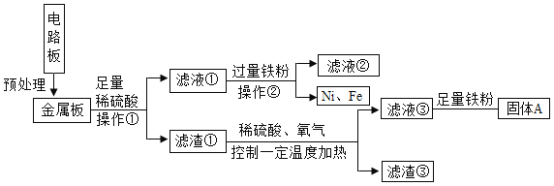
�ش��������⡣
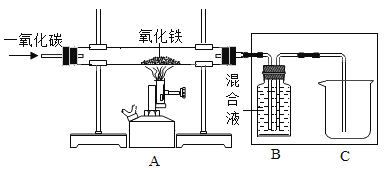
��1���������У�ʹ�õIJ����������ձ����������⣬����______________��
��2���������к��еĽ�����_______________��
��3����Һ���м����������۵���ҪĿ����________________������A����Ҫ����ͭ�⣬������һ����������Ϊ�˽����ᴿͭ�����������A�м���������ϡ���ᣬ������Ӧ�Ļ�ѧ����ʽΪ________________��
��4�������ֱ�ӷ��շϾɵ�·����ս������ù������̵���Ҫ�ŵ���__________��
(��)�������������Ļ��ǿ����̽����
��������ͭ���ճ�������ʹ�������Ľ�����ij��ѧ��ȤС���ҵ���������ͭ�����ֽ�������������ʵ�顣

��1���������ִ�ĥ��������ͼ����ʵ�飬����������ͬŨ�ȵ�ϡ���ᣬ������������������ݵĿ�����Ϊ�����ж������ֽ����Ļ��ǿ������ͬѧ��Ϊ����������������_______________��
��2����ʦ������ȤС��ij�Ա��ֻҪ����һ���Լ����Ϳ�ͨ��ʵ������Ͷ�Ӧ����ó������ֽ������ǿ����˳�������������Լ��з���Ҫ�����_______________��������ĸ��
Aϡ����
B��������Һ
C����������Һ
���𰸡�ˮ������ �ӿ�������ʴ ©�� Ag ��ͭ�û����� Fe + H2SO4 = FeSO4 + H2�� �����˻�����Ⱦ ��������ĽӴ��������ͬ C
��������
(һ)����Ʒ�ķ���
��1��������Ҫ�ɷ���Fe2O3�qxH2O����������Ҫ������е�ˮ�������йأ�
��2����ͼ1ʵ��˵��NaCl���������е������Ǽӿ�������ʴ��
(��)�����Ļ�������
��1�����˲������Խ������Թ������Һ�з���������������У�ʹ�õIJ����������ձ����������⣬����©����
��2��ͭ��������ϡ�����ڼ��ȵ���������������ͭ��ˮ�������������к��еĽ�����Ag��
��3�����Ļ������ͭ��ǰ�棬��Һ���м����������۵���ҪĿ���ǣ���ͭ�û�����������ϡ���ᷴӦ����������������������ѧ����ʽΪ��Fe + H2SO4 = FeSO4 + H2��
��4��ֱ�ӷ��շϾɵ�·����ս����������Ⱦ�����壬���Ըù������̵���Ҫ�ŵ��ǣ������˻�����Ⱦ��
(��)�������������Ļ��ǿ����̽����
��1���������ִ�ĥ��������ͼ3����ʵ�飬����������ͬŨ�ȵ�ϡ���ᣬ�ԡ���������������ݵĿ�����Ϊ�����ж������ֽ����Ļ��ǿ������ͬѧ��Ϊ���������������ǽ�������ĽӴ��������ͬ��
��2��A�����ڽ�������ĽӴ��������ͬ������ͨ���Ƚ������ᷴӦ�����ʣ��ж������ֽ����Ļ��ǿ�������������⣻
B����������ͭ����������������Һ��Ӧ�����Բ��ܱȽϳ�˳���������⣻
C������������������Һ��Ӧ��˵�����������ã�ͭ����������������Ӧ��˵��ͭ���������ã��ܱȽϳ�˳�������⡣��ѡC��

 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�����Ŀ�������̽����������ͭ�Ļ��ǿ��������������ݡ�
[���ʵ��]
��� | ���� | ���� | ���� |
�� | ������δ��ĥ����˿����CuSO4��Һ�� | ���������� | |
�� | �������ĥ�����˿����CuSO4��Һ�� | ��˿����������ɫ���� | ��ѧ����ʽΪ:____________, |
�� | ������δ��ĥ����˿����CuCl2��Һ�� | ��˿��������__________ɫ���� |
|
��1����˿������һ������Ĥ�����γɵ�ԭ����(�û�ѧ����ʽ��ʾ)________________��
��2���Ƚ�ʵ���Һ�ʵ��________________(����������������)�ɵ�֪:��ĥ���ƻ���������Ĥ��
[�����뷴˼]
��1���ݴ˿�֪�������Al��Cu_______________(����ǿ���� ������)��
��2���������ϵ�֪: CuSO4 ��Һ����Cu2+��SO42-��H2O�������ӣ�CuCl2��Һ����Cu2+��CI-��H2O�������ӡ�С��ͬѧ��ʵ�����������з���������Ϊ�����IJ�����______________��
AH2O �ƻ�����������Ĥ
BCl- �ƻ�����������Ĥ
CCu2+ �ƻ�����������Ĥ
DSO42-�ƻ�����������Ĥ
����Ŀ����һ�ܱ���������CO2��H2O��O2������R����һ�������³��ȼ�գ���÷�Ӧǰ������ʵ��������������˵����ȷ����
���� | R | O2 | CO2 | H2O |
��Ӧǰ����/g | 2.3 | 10.0 | 0.3 | 0.5 |
��Ӧ������/g | 0 | 5.2 | 4.7 | x |
A.x��ֵΪ3.7
B.R�Ļ�ѧʽΪC2H6
C.�÷�Ӧ���ڷֽⷴӦ
D.�÷�Ӧ��CO2��H2O�Ļ�ѧ������֮��Ϊ2��3