题目内容
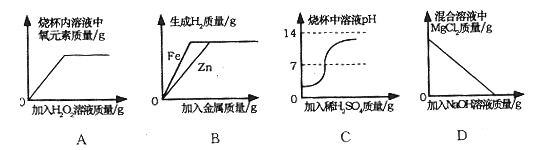
【题目】甲、乙、丙三种物质的溶解度曲线如下图所示,请根据图回答下列问题:
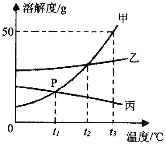
⑴P点表示的含义是________________。
⑵t2℃时,将丙物质的不饱和溶液变成饱和溶液,在不改变溶质质量分数的前提下,可采取的方法________________。
⑶t3℃时,将甲和乙两种物质的饱和溶液各100g分别蒸发10g水,然后降温到t2℃,所得溶液中溶质质量关系是甲________________乙(填“>”、“<”或“=”)。
⑷下列说法正确的是________________(填字母序号)。
A t2℃时,甲、乙两种物质的溶液溶质质量分数一定相等
B t3℃时,配制300g甲的饱和溶液,需要固体甲的质量为100g
C t3℃时,甲、乙两种物质的饱和溶液降温到t1℃,甲析出的晶体一定比乙多
D t1℃时,将等质量的甲、乙、丙三种物质制成该温度下的饱和溶液,所需溶剂的质量甲=丙>乙
【答案】t1℃时,甲和丙两种物质溶解度相等 升高温度 < BD
【解析】
(1)由图可知,P点是甲、丙两种物质的溶解度曲线在温度为t1℃时的交点,其含义是t1℃时,甲和丙两种物质溶解度相等,故填t1℃时,甲和丙两种物质溶解度相等。
(2)在不改变溶质质量分数的前提下,将丙物质的不饱和溶液变成饱和溶液,可以通过减小溶解度的途径来实现,而丙的溶解度随温度升高反而减小,所以采取的方法是升高温度,故填升高温度。
(3)由图可知,t3℃时甲的溶解度大于乙的溶解度,所以此时甲溶液的溶质质量分数大于乙溶液的溶质质量分数,甲和乙两种物质的饱和溶液各100g,则甲溶液中溶剂的质量少一点,蒸发10g水,然后降温到t2℃时,两种物质的溶解度相同,所得饱和溶液的溶质质量分数相同,所以所得甲溶液中的溶质质量小于乙溶液中溶质的质量,故填<。
(4)A 由图可知, t2℃时,甲、乙两种物质的溶解的相同,所以甲、乙两种物质的饱和溶液的溶质质量分数一定相等,题目中未指明两种溶液的状态,无法判断两种溶液中溶质质量的关系,选项错误;
B t3℃时,甲的溶解度未50g,即50g甲溶解到100g水中能写出150g饱和溶液,所以配制300g甲的饱和溶液,需要固体甲的质量为100g,选项正确;
C 给饱和溶液降低温度析出晶体,得到的晶体质量除与溶解度受温度影响方式有关,还与溶液的质量有关,t3℃时,甲、乙两种物质的饱和溶液降温到t1℃,由于两种溶液的质量关系不确定,所以甲析出的晶体不一定比乙多,选项错误;
D t1℃时,甲、乙、丙三种物质的溶解度的关系为乙>甲=丙,所以将等质量的甲、乙、丙三种物质制成该温度下的饱和溶液,所需溶剂的质量甲=丙>乙,选项正确,故填BD。

 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】某碳酸钠样品中含有一定量的碳酸氢钠。为测定其纯度,取100 g样品加热至不再产生气体(2NaHCO3![]() Na2CO3 + H2O +CO2↑),使生成的二氧化碳完全被碱石灰吸收,测得加热时间和碱石灰质量增加的关系如下表:
Na2CO3 + H2O +CO2↑),使生成的二氧化碳完全被碱石灰吸收,测得加热时间和碱石灰质量增加的关系如下表:
时间 | 0分钟 | 1分钟 | 2分钟 | 3分钟 | 4分钟 |
仪器和碱石灰的质量总和(g) | 150 | 151.5 | 153 | 154.4 | 154.4 |
(1)当完全反应后,生成二氧化碳的质量为_____g
(2)样品中碳酸钠的质量分数是_____(写出计算过程)
(3)取另一品牌的碳酸钠样品(也含一定量的碳酸氢钠)29.6g与100g18.25%的稀盐酸恰好完全反应,将溶液蒸干可得晶体的质量为________g。
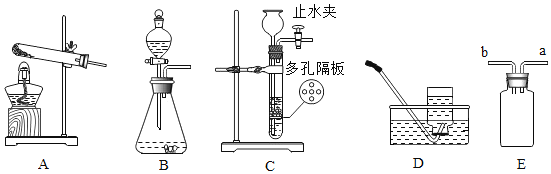
【题目】甲同学用如图所示装置制得CO2,并验证CO2性质的实验。
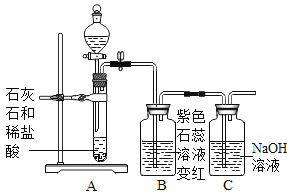
(1)制取二氧化碳反应的化学方程式是_____。
(2)乙同学在实验时闻到制得的CO2有些刺激性气味,于是乙同学对气味的来源以及能使紫色石蕊溶液变红的酸性物质产生了疑问。
(乙同学的猜想)甲同学用的盐酸浓度大或者产生气体流速大导致氯化氢逸出。
甲、乙两同学经过认真设计、反复思考,设计如下实验来解决乙同学的疑问:
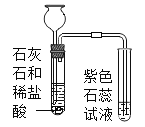
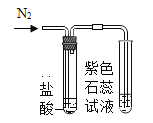
(进行实验)实验装置如下(两个实验中所用盐酸及紫色石蕊溶液与上图中所用的盐酸和石蕊溶液一样,且酸的体积和石蕊的体积都相同,夹持装置已略去)。
实验1 | 实验2 |
|
|
紫色石蕊试液变红 | 紫色石蕊试液无变化 |
(实验解释)
①乙同学进行猜想与假设的依据是_____。
②老师提示如果用实验1制取二氧化碳并验证二氧化碳与水反应,需要在两个试管之间增加装置。该装置的作用是_____,该装置中盛放的药品应具有的性质是_____。
③实验2的结论是_____。
(3)上图的C装置是想验证二氧化碳与氢氧化钠反应,实验过程中看到瓶内不断有气泡产出,但溶液始终没有明显变化,所以得不到正确的结论。
实验结束后,老师把A试管中的液体全部倒入C瓶,发现开始有气泡产生,后来产生白色沉淀。产生沉淀反应的化学方程式是_____。由此间接证明了二氧化碳能与氢氧化钠能反应
(实验结论)二氧化碳能与水、氢氧化钠反应。
(反思)实验室制取二氧化碳只能用稀盐酸,用浓盐酸的后果是_____。