题目内容
【题目】请参与探究金属铝和铜的活动性强弱,完成下列内容。
[设计实验]
编号 | 操作 | 现象 | 解释 |
甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 | |
乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 | 化学方程式为:____________, |
丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出__________色固体 |
|
(1)铝丝表面有一层氧化膜,其形成的原因是(用化学方程式表示)________________。
(2)比较实验乙和实验________________(填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
[结论与反思]
(1)据此可知金属活动性Al比Cu_______________(填“强”或 “弱”)。
(2)查阅资料得知: CuSO4 溶液中有Cu2+、SO42-、H2O三种粒子,CuCl2溶液中有Cu2+、CI-、H2O三种粒子。小明同学对实验丙的现象进行分析,你认为合理的猜想是______________。
AH2O 破坏了氧化铝薄膜
BCl- 破坏了氧化铝薄膜
CCu2+ 破坏了氧化铝薄膜
DSO42-破坏了氧化铝薄膜
【答案】![]() 红
红 ![]() 甲 强 B
甲 强 B
【解析】
[设计实验]
乙将表面打磨后的铝丝浸入CuSO4溶液中,铝丝表面析出红色固体,也就是铝与硫酸铜发生反应生成硫酸铝和铜,化学方程式是![]() ;
;
故填:![]() 。
。
丙将表面未打磨的铝丝浸入CuCl2溶液中,铝与氯化铜溶液发生了反应,现象是铝丝表面析出红色的固体;
故填:红色。
(1)铝丝表面有一层氧化膜,是铝与空气中的氧气反应生成氧化铝,化学方程式是![]() ;
;
故填:![]() 。
。
(2)甲将表面未打磨的铝丝浸入CuSO4溶液中,乙将表面打磨后的铝丝浸入CuSO4溶液中,比较实验乙和实验甲,打磨能破坏氧化铝薄膜;
故填:甲。
[结论与反思]
(1)通过实验,铝能把铜从铜的化合物溶液中置换出来,可知金属活动性Al比Cu强;
故填:强。
(2)甲同学的实验中,将表面未打磨的铝丝浸入CuSO4溶液中,CuSO4溶液中有Cu2+、SO42-、H2O三种粒子,但没有发生反应,丙同学将表面未打磨的铝丝浸入CuCl2溶液中,CuCl2溶液中有Cu2+、CI-、H2O三种粒子,但发生化学反应,故合理的猜想是Cl-破坏了氧化铝薄膜;
故选:B。

 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1),溶于水后有许多气泡产生(如图2).该小组同学进行如下探究。
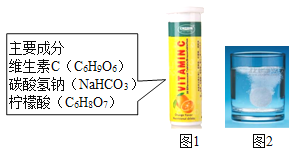
[提出问题]该气体的成分是什么?
该气体不可能含有SO2,因为________。
[提出猜想]Ⅰ.CO2 Ⅱ.__________。 Ⅲ.CO2和O2
[进行实验]
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 将气体通入________。 | _________。 | 该气体含有CO2,方程式是________。 |
(2) | 将带火星的木条伸入该气体中。 | 带火星的木条没有复燃。 | 该气体不是纯氧气。 |
[得出结论]该气体含有CO2_______(填“能”或“不能”)确定该气体中是否含氧气,理由是_________。
[讨论交流]维C泡腾片溶液是否呈酸性。向维C泡腾片溶液中滴加________试剂,溶液_______,说明该溶液显酸性。