题目内容
【题目】在一密闭容器中有CO2、H2O、O2和物质R,在一定条件下充分燃烧,测得反应前后各物质的质量如表。下列说法正确的是
物质 | R | O2 | CO2 | H2O |
反应前质量/g | 2.3 | 10.0 | 0.3 | 0.5 |
反应后质量/g | 0 | 5.2 | 4.7 | x |
A.x的值为3.7
B.R的化学式为C2H6
C.该反应属于分解反应
D.该反应中CO2与H2O的化学计量数之比为2∶3
【答案】D
【解析】
在化学反应中随着反应的进行反应物的质量会不断减少,生成物的质量会增加,根据表格提供的数据,R的质量由2.3g变为0,减少2.3g,是反应物;O2的质量由10.0g变为5.2g,减少4.8g,是反应物;CO2的质量由0.3g变为4.7g,增加4.4g,是生成物;H2O的质量由0.5g变为3.2g(根据质量守恒定律计算得出),增加2.7g,是生成物。因此该反应是R和氧气反应生成二氧化碳和水。
A、根据质量守恒定律,反应前后物质的总质量相等,则2.3g+10.0g+0.3g+0.5g=0+5.2g+4.7g+x,解得x=3.2g,选项A不正确;
B、根据质量守恒定律,反应前后元素的种类不变,元素的质量也不变。生成的CO2中碳元素质量为:![]() ,氧元素的质量为:4.4g-1.2g=3.2g;生成的水中氢元素的质量为:
,氧元素的质量为:4.4g-1.2g=3.2g;生成的水中氢元素的质量为:![]() ,氧元素的质量为:2.7g-0.3g=2.4g;而参加反应的氧气质量为4.8g,因此R中含碳元素质量:1.2g,氢元素质量:0.3g,氧元素质量:3.2g+2.4g-4.8g=0.8g。据此计算结果可得出R的化学式为C2H6O,选项B不正确;
,氧元素的质量为:2.7g-0.3g=2.4g;而参加反应的氧气质量为4.8g,因此R中含碳元素质量:1.2g,氢元素质量:0.3g,氧元素质量:3.2g+2.4g-4.8g=0.8g。据此计算结果可得出R的化学式为C2H6O,选项B不正确;
C、根据分析结果,该反应的反应物和生成物都是两种,不符合分解反应的定义,选项C不正确;
D、根据分析结果,该反应中生成的CO2与H2O的质量比为4.4g和2.7g,假设CO2和H2O化学式前的化学计量数分别为a和b,则![]() ,解得
,解得![]() ,因此该反应中CO2与H2O的化学计量数之比为2∶3,选项D正确。故选D。
,因此该反应中CO2与H2O的化学计量数之比为2∶3,选项D正确。故选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
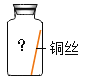
小学生10分钟应用题系列答案【题目】某些铜制品在空气中久置表面会生成绿色的铜锈,其主要成分为Cu2(OH)2CO3,现探究铜生锈的条件。
[提出猜想]根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2共同作用有关。
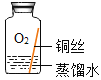
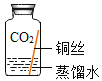
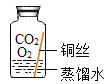
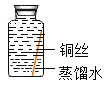
[进行实验]实验小组取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
[解释与结论]
(1)根据对比实验①和③,得出的结论是_____。
(2)从优化实验的角度考虑,实验_____(填编号)为多余。
(3)为验证猜想,请将图中实验⑤补充完整_____。
(4)由上述实验可推知,猜想正确。
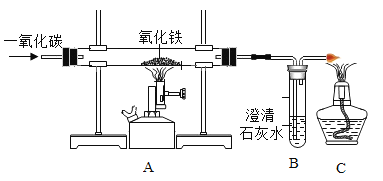
【题目】某中学化学兴趣小组通过实验测定某大理石中碳酸钙的质量分数。将盛有一定量该样品的烧杯放在电子秤上,倒入100.0g稀盐酸(假设大理石样品中的杂质不与稀盐酸反应,也不溶于水),使该样品完全反应,已知烧杯的质量为60.0g,实验过程中的有关数据如下表:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯与所盛物质质量/g | 186.0 | 183.0 | 181.0 | 180.0 | 179.4 | 179.4 |
试计算:
(1)碳酸钙中碳元素与氧元素的质量比(最简比)为_________。
(2)生成二氧化碳的质量为_________g。
(3)求该大理石中碳酸钙的质量分数___________(精确到0.1%)。