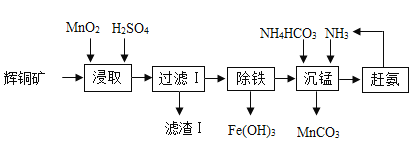
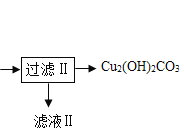
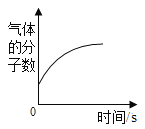
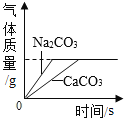
��Ŀ����
����Ŀ���ҹ�����úΪ��Ҫȼ�ϵĴ��������������������ú��Ϊȼ���йء�úȼ�����ɵ�SO2���������Ҫ��Ⱦ�
��1����ҵ�ϳ�����ʯ�ң�CaO��Ϊ�������������������е�SO2��O2��������CaSO4����Ӧ����ʽΪ________________________��
��2��ijͬѧ�����кͷ�Ӧ��ԭ��ģ������SO2ͨ������KOH��Һ�У���̽����Ӧ����Һ�����ʵijɷ֡�
�����ϣ�������������ʹ����KMnO4��Һ��ɫ���ڳ����£������ܰ������ἰ������������������������Σ�����������̼�����ƣ��ڳ������ֽ⡣
�����룩����K2SO3������K2SO4������________________��
���������飩
���� | ʵ����� | ʵ������ | ���� |
�� | ȡһ������Ӧ�����Һ��A��B��ֻ�Թ��� | ||
�� | ��A�Թ��е��뼸������KMnO4��Һ�� | ________�� | ֤����K2SO3�� |
�� | ��B�Թ��е���������ϡ���ᣬ�ټ���_______�� | �а�ɫ�������� | ֤����________�� |
�������жϣ�����________������
����չ��ʵ��۳��������ķ�Ӧ����ʽ��________________________________________��
���𰸡�![]() K2SO3��K2SO4 ��ɫ��Һ��ɫ BaCl2��Һ K2SO4 III
K2SO3��K2SO4 ��ɫ��Һ��ɫ BaCl2��Һ K2SO4 III ![]()
��������
��1�������ƺͶ�������������Ӧ��������ƣ���ѧ����ʽΪ��![]() ��
��
��2����SO2ͨ������KOH��Һ�У���Ӧ����Һ�����ʿ�����������أ�Ҳ����������أ�Ҳ������������غ�����صĻ���ȡһ������Ӧ�����Һ��A��B��ֻ�Թ��У���A�Թ��е��뼸������KMnO4��Һ����ɫ��Һ��ɫ����֤����K2SO3����B�Թ��е���������ϡ���ᣬ�ټ���BaCl2��Һ���а�ɫ�������ɣ���֤����K2SO4������III������ʵ���������غ��Ȼ�����Ӧ�������ᱵ�������Ȼ��أ���ѧ����ʽΪ��![]() ��
��

 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д�