题目内容
【题目】下面是几种实验室制取气体的发生装置和收集装置。请回答下列问题:
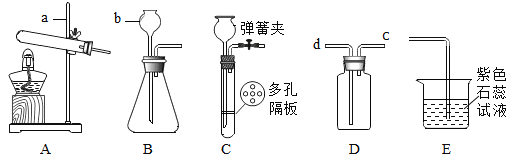
①请写出标有序号的仪器的名称:a_____;b_____。
②小华同学用浓盐酸与大理石在C装置中反应,制取CO2后通入到盛有紫色石蕊试液的烧杯E中,观察到紫色石蕊试液变红,对这一现象的解释合理的是_____。
a、产生的CO2直接使石蕊变红
b、挥发出的氯化氢气体溶于水,使石蕊试液变红
c、产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
③采用装置A加热氯酸钾和二氧化锰的混合物制取氧气,若用D装置采用排空气法收集氧气,氧气应从_____(选填“c”或“d”)进。
④实验室加热氯酸钾和二氧化锰的混合物28.0g制取氧气,完全反应后剩余固体质量为18.4g,请计算:
I、生成氧气的质量为_____g。
II、求原混合物中氯酸钾的物质的量_____。(根据化学方程式列式计算)
【答案】铁架台 长颈漏斗 bc d 9.6 0.2mol
【解析】
①根据常用仪器可知①是铁架台、②是长颈漏斗,故填写:铁架台;长颈漏斗;
②酸可以使石蕊试液变红,小华同学用浓盐酸和大理石在C装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红.可能的原因有:产生的CO2与水反应生成H2CO3使石蕊试液变红;挥发出的氯化氢溶于水使石蕊试液变红,故填写:bc;
③氧气的密度略大于空气,可采用向上排空气法收集,D装置瓶口向上,应该长导管进气,短导管出气,故填写:d;
④I、根据质量守恒定律可得,生成的氧气的质量为28.0g-18.4g=9.6g,故填写:9.6;
II、设原混合物中氯酸钾的质量为x

原混合物中氯酸钾的物质的量为:
答:原混合物中氯酸钾的物质的量为0.2mol。

【题目】我国是以煤为主要燃料的大国,北京的雾霾天气与煤作为燃料有关。煤燃烧生成的SO2是酸雨的主要污染物。
(1)工业上常以生石灰(CaO)为脱硫剂,高温下与废气中的SO2、O2化合生成CaSO4,反应方程式为________________________。
(2)某同学利用中和反应的原理模拟脱硫,将SO2通入足量KOH溶液中,并探究反应后溶液中溶质的成分。
(资料)①亚硫酸盐能使酸性KMnO4溶液褪色;②常温下,硝酸能把亚硫酸及亚硫酸盐氧化成硫酸和硫酸盐;③亚硫酸与碳酸相似,在常温下易分解。
(猜想)(Ⅰ)K2SO3;(Ⅱ)K2SO4;(Ⅲ)________________。
(进行试验)
步骤 | 实验操作 | 实验现象 | 结论 |
① | 取一定量反应后的溶液于A、B两只试管中 | ||
② | 向A试管中滴入几滴酸性KMnO4溶液。 | ________。 | 证明有K2SO3。 |
③ | 向B试管中滴入足量的稀盐酸,再加入_______。 | 有白色沉淀生成 | 证明有________。 |
(作出判断)猜想________成立。
(拓展)实验③沉淀产生的反应方程式是________________________________________。
【题目】某白色固体由BaCl2,NaOH、Na2CO3、Na2SO4中的一种或几种物质组成,某兴趣小组为确定其成分,进行了如下实验探究。
Ⅰ.初步探究:小金同学设计的实验过程及现象如下图所示
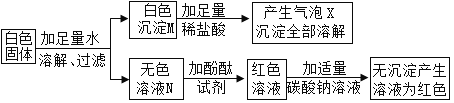
(查阅资料)BaCl2溶液显中性,BaSO4沉淀不溶于稀硝酸等酸。
(初步分析)(1)白色沉淀M的化学式是________________,产生气体X的化学方程式是_______________
(2)溶液N中的溶质一定有_____________________,一定没有氯化钡。
(3)原白色固体中一定有的物质是____________,一定没有的物质是_________________。
(交流讨论)小英同学认为:无色溶液N滴加酚酞试液后变红,说明溶液N中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠,若要进一步确定,需对溶液N继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液N中有氢氧化钠吗?
(猜想与假设)猜想1:有NaOH;猜想2:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
取无色溶液N加入过量BaCl2溶液,振荡后静置 | ______ | 证明溶液N中有碳酸钠并已被除尽 |
取上述步骤所得上层清液于试管中,加入________ | _______ | 猜想1正确 |
【题目】生石灰常用作食品干燥剂,干燥剂的包装袋上除了标明主要成分为生石灰外,还提醒人们注意:不可食用、不可浸水、不可开袋、不可玩耍、儿童勿取。
(1)同学们将一袋 干燥剂倒入一定 量的水中,发现生石灰开始“沸腾”,咕嘟咕嘟冒泡,不时有水蒸汽冒出,充分搅拌后过滤,得到白色沉淀和滤液。通过实验现象可知生石灰遇水会_____________(选填“吸热”或“放热”),写出有关反应的化学方程式:_________________。
(2)同学们想知道所得白色沉淀的成分,进行了如下探究:
[提出问题]白色沉淀中含有哪些物质?
[猜想假设]猜想1:只含有氢氧化钙;
猜想2:只含碳酸钙;
猜想3:_________________。
[实验探究]同学们进行了如下表所示的实验,请将下表填写完整;
实验步骤 | 现象现象 | 结论 |
I.取少量样品于试管中,加入足量的稀盐酸 | ______________ | 猜想1不成立 |
II.另取少量样品于试管中,加入适量水,充分搅拌后,滴加______________________ | 溶液呈红色 | 猜想3成立 |
[拓展延伸]①写出步骤I中发生反应的化学方程式:_________________。
②实验室正确保存生石灰的方法是_________________。